题目内容
8. 小明对实验室用石灰石和稀盐酸制取二氧化碳后的废液,进行溶质成分鉴定.取废液上层清液50克,逐滴加入质量分数为10.6%的碳酸钠溶液,出现气泡,滴加至20克开始出现白色沉淀.继续滴加至沉淀不再产生,过滤,测得沉淀的质量为5克,并绘制了图象.
小明对实验室用石灰石和稀盐酸制取二氧化碳后的废液,进行溶质成分鉴定.取废液上层清液50克,逐滴加入质量分数为10.6%的碳酸钠溶液,出现气泡,滴加至20克开始出现白色沉淀.继续滴加至沉淀不再产生,过滤,测得沉淀的质量为5克,并绘制了图象.(1)碳酸钠属于盐(选填“盐”或“碱”).
(2)废液中含有的溶质是HCl、CaCl2(写化学式).
(3)图象中的a点数值是0.88.
(3)通过计算说明,图象横坐标中的b点表示的溶液的质量是多少克?
分析 根据化学方程式计算的步骤有:一设、二写、三找、四列、五答、六查.由图象可知:废液中含有的溶质是氯化氢和氯化钙的混合物;滴加的溶液中溶质是碳酸钠,属于盐;20克碳酸钠溶液与质量分数的乘积是溶质的质量;图象中的a点数值是二氧化碳的质量,可以根据碳酸钠的质量求出;图象横坐标中的b点表示的溶液的质量可以根据化学方程式的计算求出.
解答 解:(1)碳酸钠由钠离子和碳酸根离子构成,属于盐,故答案为:盐;
(2)由图象可知:废液中含有的溶质是氯化氢和氯化钙的混合物,注意写化学式,故答案为:HCl、CaCl2;
(3)a点时加入碳酸钠溶液中溶质的质量=20g×10.6%=2.12g,
图象中的a点数值是二氧化碳的质量,可以根据碳酸钠的质量求出;设二氧化碳的质量为x
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
2.12g x
$\frac{106}{2.12g}=\frac{44}{x}$
x=0.88g
故答案为:0.88;
(5)设与氯化钙反应的碳酸钠溶液中溶质质量为y,
CaCl2+Na2CO3=2NaCl+CaCO3↓
106 100
y 5g
$\frac{106}{y}=\frac{100}{5g}$
y=5.3g
溶液质量是$\frac{5.3g}{10.6%}$=50g
b点质量应标20g+50g=70g
故答案为:70g.
点评 本考点考查了根据化学方程式的计算,属于质量分数和化学方程式的综合应用,是中考计算题中经常出现的题型.做题时要注意:化学方程式要写正确,始终不要忘记质量守恒定律,本考点主要出现在计算题中.

 阅读快车系列答案
阅读快车系列答案| A. | C→CO2 | B. | CO2→H2CO3 | C. | H2CO3→CaCO3 | D. | CaCO3→Ca(OH)2 |
 如图表示两种物质发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合.下列说法中错误的是( )
如图表示两种物质发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合.下列说法中错误的是( )| A. | 该反应属于置换反应 | B. | 该反应前后分子个数不变 | ||
| C. | 该反应中有三种元素参与 | D. | 该反应的生成物均为化合物 |
| 物 质 | 选 用 试 剂 及 操 作 方 法 | |
| A | Cu(CuO) | 加入足量的稀硫酸,在充分反应后过滤. |
| B | O2(CO2) | 通入足量的氢氧化钠溶液,充分反应后干燥 |
| C | CaCl2溶液(盐酸) | 加入足量的碳酸钙粉末,充分反应后过滤 |
| D | CuSO4(FeSO4) | 加入过量的铁粉,充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 将CuSO4溶液加水稀释 | B. | 观察Cu( NO3)2溶液 | ||
| C. | 观察Na2SO4 | D. | 向CuSO4溶液中滴加足量NaOH溶液 |
 完成下列各题:
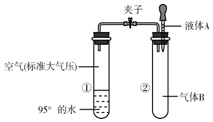
完成下列各题: 如图,试管中加入硝酸铵固体片刻后,U 型管左侧液面将上升(填“上升”、“下降”或“不变”),产生这一现象的原因是硝酸铵溶于水后吸热温度降低,导致集气瓶内气压降低瓶内压强变小.
如图,试管中加入硝酸铵固体片刻后,U 型管左侧液面将上升(填“上升”、“下降”或“不变”),产生这一现象的原因是硝酸铵溶于水后吸热温度降低,导致集气瓶内气压降低瓶内压强变小.

