题目内容
18.我国科学家屠呦呦发现并提纯抗疟疾药物青蒿素(C15H22O5)荣获 2015年诺贝尔奖.请计算:(1)青蒿素(C15H22O5)的相对分子质量;
(2)青蒿素中碳、氢、氧元素的质量比.
分析 (1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析判断;
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
解答 解:(1)青蒿素的相对分子质量是12×15+1×22+16×5=282;
(2)青蒿素中碳、氢、氧三种元素的质量比为(12×15):(1×22):(16×5)=90:11:40;
故答案为:(1)282;(2)90:11:40.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
9.下列对图示实验现象的描述中,不正确的是( )
| A. | 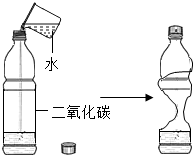 旋紧瓶盖振荡, 旋紧瓶盖振荡,塑料瓶变瘪 | |
| B. | 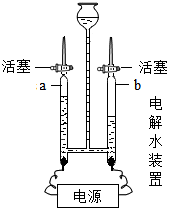 用燃着的木条 用燃着的木条a管尖嘴口检验 产生的气体,木条 燃烧更旺 | |
| C. |  黄铜片在纯铜片 黄铜片在纯铜片上刻画时留下痕迹 | |
| D. | 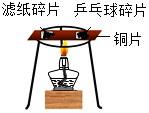 滤纸碎片先燃烧,乒乓球碎片后燃烧 滤纸碎片先燃烧,乒乓球碎片后燃烧 |
3.下列各组物质的化学名称或俗称和化学式表示同一种物质的是( )
| A. | 烧碱 纯碱 NaOH | B. | 氧化钙 消石灰 CaO | ||
| C. | 氢氧化钙 熟石灰 Ca(OH)2 | D. | 冰 干冰 H2O |
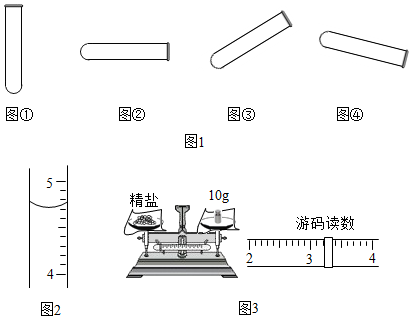
 人体缺乏维生素C(简写“Vc”)就会患坏血病.如图所示为某种“维生素C”说明书的一部分.
人体缺乏维生素C(简写“Vc”)就会患坏血病.如图所示为某种“维生素C”说明书的一部分.