题目内容
某校化学小组的同学想探究生铁中碳的含量,他们取组成完全相同的三份生铁(假设生铁中只含铁和碳),分别加入50 g稀硫酸中进行实验(实验Ⅰ、Ⅱ、Ⅲ),充分反应后得到下表的实验数据:
| 实验次数 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
| 生铁的质量/g | 2.9 | 5.8 | 7.2 |
| 氢气的质量/g | 0.1 | 0.2 | 0.2 |
请计算:(计算结果精确到0.1%)
(1)该生铁中碳的质量分数为________。
(2)所用稀硫酸的溶质质量分数是多少?
(1)3.4%
(2)由表中数据分析可知,实验Ⅱ中50 g稀硫酸已完全反应。
解:设50 g稀硫酸中含H2SO4的质量为x。
Fe+H2SO4===FeSO4+H2↑
98 2
x 0.2 g
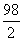 =
=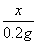 解得:x=9.8 g
解得:x=9.8 g
所用稀硫酸的溶质质量分数=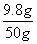 ×100%=19.6%
×100%=19.6%
答:略。

练习册系列答案
相关题目
某校化学小组的同学想探究生铁中碳的含量,他们取组成完全相同的三份生铁(假设生铁中只含铁和碳),分别加入50g稀硫酸中进行实验(实验I、Ⅱ、Ⅲ),充分反应后得到下表的实验数据:请计算:(计算结果精确到0.1%):
(1)该生铁中碳的质量分数为______.
(2)所用稀硫酸的溶质质量分数是多少?
| 实验次数 | 实验I | 实验Ⅱ | 实验Ⅲ |
| 生铁的质量 | 2.9g | 5.8g | 7.2g |
| 氢气的质量 | 0.1g | 0.2g | 0.2g |
(2)所用稀硫酸的溶质质量分数是多少?
某校化学小组的同学想探究生铁中碳的含量,他们取组成完全相同的三份生铁(假设生铁中只含铁和碳),分别加入50g稀硫酸中进行实验(实验I、Ⅱ、Ⅲ),充分反应后得到下表的实验数据:请计算:(计算结果精确到0.1%):
(1)该生铁中碳的质量分数为______.
(2)所用稀硫酸的溶质质量分数是多少?
| 实验次数 | 实验I | 实验Ⅱ | 实验Ⅲ |
| 生铁的质量 | 2.9g | 5.8g | 7.2g |
| 氢气的质量 | 0.1g | 0.2g | 0.2g |
(2)所用稀硫酸的溶质质量分数是多少?