题目内容
4.火柴是一种日常用品,它在点燃过程中发生的是化学变化,判断的依据是有新物质生成.火柴在燃烧过程还可以看到发出白光,闻到刺激性气味,手会感觉到发烫,以上现象都可以帮助我们判断是否发生了化学变化.分析 根据生成其他物质的变化叫化学变化,又叫化学反应,它的本质特征是有其他(新的)物质生成,还伴随有发光、发热、有味等现象,依此进行分析解答本题.
解答 解:火柴在点燃过程中发生的是变化,判断依据是看到有新物质生成,火柴在燃烧过程还可以看到白光,闻到有刺激性气味,手会感觉到发烫、发热;
故答案为:化学;有新物质生成;发出白光;刺激性气味;发烫.
点评 本题考查了火柴与氧气的反应,完成此题,可以依据已有的知识进行.

练习册系列答案
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
14.下列除去杂质的方法中正确的是( )
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | CaCl2溶液 | 稀盐酸 | 加过量碳酸钙,过滤 |
| B | K2CO3溶液 | KCl | 加适量稀盐酸 |
| C | CaO | CaCO3 | 加水,过滤 |
| D | NaCl溶液 | Na2CO3 | 加适量硝酸钙溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
19.下列叙述中,错误的是( )
| A. | 空气中的氧气主要来自于植物的光合作用 | |
| B. | 氧化反应就是物质与氧气发生的反应 | |
| C. | 用含有氧元素的物质才有可能产生氧气 | |
| D. | 工业上获得大量氮气是从空气中得到的 |
9.阳光中学的同学从山上采集到一种石灰石(主要成分是碳酸钙),他们取80g该石灰石样品进行煅烧实验(杂质不变化),测得反应后固体质量(m)与时间的关系如下表:
(1)当石灰石完全反应时,生成二氧化碳的质量为22 g.
(2)该该石灰石样品中CaCO3的质量分数(百分含量)是多少?(Ca 40,O 16,C 12)
| 反应时间(分钟) | 0 | 3 | 5 | 7 | 8 | 9 | 10 |
| 反应后固体质量g | 80 | 75 | 70 | 66 | 62 | 58 | 58 |
(2)该该石灰石样品中CaCO3的质量分数(百分含量)是多少?(Ca 40,O 16,C 12)
13.分别将下列各组物质同时加到水中,能得到无色透明溶液的是( )
| A. | CuSO4、HCl | B. | H2SO4、BaCl2 | C. | FeCl3、KOH | D. | Na2SO4、HNO3 |
14.2015年央视“3•15晚会”爆光山东一些非法炼油厂生产有毒调和汽油,用90号汽油、石脑油、芳烃、甲缩醛等混合而成.其中不少化工原料在国家标准中明令禁止,如甲缩醛会造成汽车漏油、挥发有害气体,污染环境等.甲缩醛分子结构模型如图,下列关于甲缩醛的说法错误的是( )
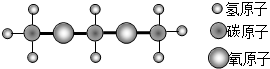

| A. | 甲缩醛化学式为C3H8O2 | |
| B. | 甲缩醛由碳、氧、氢原子构成 | |
| C. | 甲缩醛中碳元素的质量分数最大 | |
| D. | 甲缩醛碳元素与氧元素质量比为9:8 |

 煤制取乙二醇的产业化发展已被列入我国2009-2015年石化产业调整和振兴规划(煤制取乙二醇的流程如图所示).
煤制取乙二醇的产业化发展已被列入我国2009-2015年石化产业调整和振兴规划(煤制取乙二醇的流程如图所示).