题目内容
5.20℃时,将等质量的甲、乙两种固体物质,分别加人到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2,甲、乙两种物质的溶解度曲线如图3.请结合图示回答下列问题:
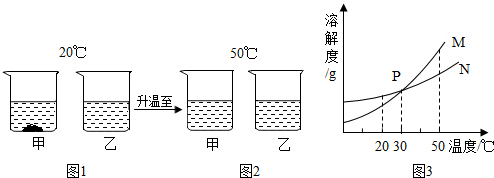
(1)图1中一定为饱和溶液的是甲溶液(填“甲”或“乙”);图2中乙溶液一定是不饱和溶液(填“饱和”或“不饱和”).
(2)图3中表示乙的溶解度曲线是N(填“M”或“N”).
(3)50℃时,甲、乙两溶液中溶质质量分数的大小关系为相等.
分析 (1)根据饱和溶液的定义进行解答;
(2)根据图中信息可以知道20℃时甲的溶解度小于乙的溶解度,结合图3可以完成解答;
(3)根据溶质质量分数公式计算即可.
解答 解:(1)从图1中可以知道甲没有完全溶解,则说明甲中形成的溶液为饱和溶液,乙完全溶解可能是饱和溶液,也可能是不饱和溶液,但是由于甲乙物质的溶解度随温度的升高而增大,所以乙溶液升温后一定变为不饱和溶液;故填:甲;不饱和;
(2)根据图1中信息可以知道20℃时甲的溶解度小于乙的溶解度,而图3中在20℃时,N曲线的溶解度大于M曲线的溶解度,故N表示的是乙物质的溶解度曲线;故填:N;
(3)50℃时,将等质量的甲、乙两种固体物质,分别加人到盛有100g水的烧杯中,甲乙物质完全溶解,溶质质量相等,溶剂质量也相等,所以50℃时,甲、乙两溶液中溶质质量分数相等.故填:相等.
点评 本题着重考查了学生对溶解度曲线知识的掌握,有利于学生分析、解决问题能力的培养.

练习册系列答案
 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
16.下列粒子结构示意图中能表示第二周期元素的是( )
| A. | 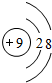 | B. |  | C. | 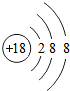 | D. | 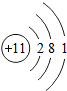 |
20.如表是氯化钠和碳酸钠在不同温度时的溶解度,根据此表回答:
①40℃时,氯化钠的溶解度为36.6g/100g水;
②碳酸钠溶液中混有少量的氯化钠,可通过降温结晶(或冷却热的饱和溶液)的方法提纯;
③碳酸钠的溶解度随温度的升高而增大(填“增大”或“减小”).在20℃时,将100g水加入30g碳酸钠中,充分搅拌后得到的是饱和(填“饱和”或“不饱和”)溶液,将上述溶液升温到30℃,该溶液的溶质质量分数为23.1%.
| 温度/℃ | 10 | 20 | 30 | 40 | |
| 溶解度 g/100gH2O | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
| 碳酸钠 | 12.2 | 21.8 | 39.7 | 53.2 | |
②碳酸钠溶液中混有少量的氯化钠,可通过降温结晶(或冷却热的饱和溶液)的方法提纯;
③碳酸钠的溶解度随温度的升高而增大(填“增大”或“减小”).在20℃时,将100g水加入30g碳酸钠中,充分搅拌后得到的是饱和(填“饱和”或“不饱和”)溶液,将上述溶液升温到30℃,该溶液的溶质质量分数为23.1%.
15.下列变化中,没有化学变化发生的是( )
| A. | 铁钉生锈 | B. | 蜡烛燃烧 | C. | 葡萄酿酒 | D. | 冰雪融化 |
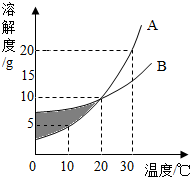 如图是A、B两种物质的溶解度曲线,请填空:
如图是A、B两种物质的溶解度曲线,请填空: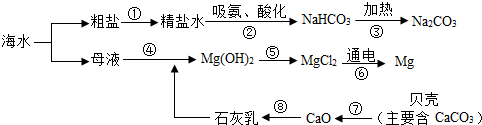

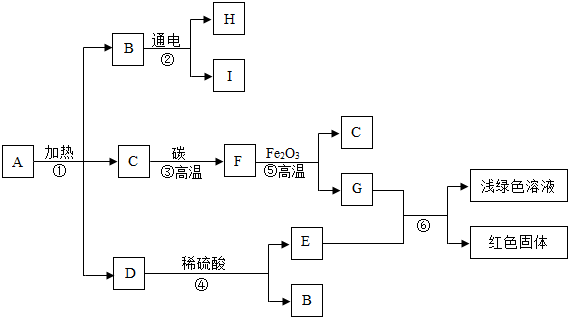
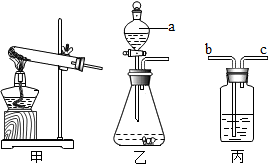 下列是实验室制备气体常用装置.
下列是实验室制备气体常用装置.