题目内容
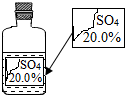 一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如图所示.要求同学们进行探究:确认这瓶溶液究竟是什么溶液?
一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如图所示.要求同学们进行探究:确认这瓶溶液究竟是什么溶液?【提出猜想】王老师提示:这瓶无色溶液只能是下列四种溶液中的一种:①硫酸镁溶液 ②硫酸钠溶液 ③硫酸溶液 ④硫酸铵溶液
【查阅资料】①常温下,相关物质的溶解度如下:
| 物质 | MgSO4 | Na2SO4 | (NH4)2SO4 | H2SO4 |
| 溶解度 | 35.1g | 19.5g | 75.4g | 与水任意比互溶 |
(1)【实验探究】小明对王老师的提示进行了评价不可能是Na2SO4,原因是
(2)为确定其它几种猜想是否正确,小明同学继续进行探究:
| 实验操作 | 实验现象 | 实验结论 |
| ①取该溶液少许于试管中,向其中滴加几滴 | 溶液中有白色沉淀生成 | 猜想①成立 |
| ②用玻璃棒蘸取少许原溶液滴在pH试纸上,并跟标准比色卡对照 | 溶液pH小于7 | 猜想③成立 |
(3)请你设计实验方案,确认该溶液是硫酸铵溶液并完成实验报告:
| 实验操作 | 实验现象 | 实验结论 |
| 取该溶液少许于试管中, ① ②将湿润的红色石蕊试纸放在试管口 | ①产生有刺激性气味的气体 ② | 猜想④成立,该反应的化学方程式为 |
考点:缺失标签的药品成分的探究,溶质的质量分数、溶解性和溶解度的关系,酸的化学性质,溶液的酸碱性与pH值的关系,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)[实验探究]根据溶解度与饱和溶液的质量分数的关系,利用饱和溶液的溶质质量分数为该温度下该溶液的溶质质量分数最大值,由硫酸钠的溶解度为19.5g而标签上标明溶液的溶质质量分数为20.0%,可判断猜想②溶液为硫酸钠溶液是不成立的;
(2)通过滴加某试剂观察到出现白色沉淀而判断溶液为硫酸镁,根据三种溶液中溶质化学性质的差异,可判断所滴加溶液应为碱溶液如氢氧化钠溶液;根据硫酸溶液和硫酸铵溶液都呈酸性的特点,可判断由pH小于7就得出溶液为硫酸溶液的说法不能成立;
(3)根据硫酸铵溶液中含有铵根的特殊性,可通过检验铵根的存在而确认溶液为硫酸铵.
(2)通过滴加某试剂观察到出现白色沉淀而判断溶液为硫酸镁,根据三种溶液中溶质化学性质的差异,可判断所滴加溶液应为碱溶液如氢氧化钠溶液;根据硫酸溶液和硫酸铵溶液都呈酸性的特点,可判断由pH小于7就得出溶液为硫酸溶液的说法不能成立;
(3)根据硫酸铵溶液中含有铵根的特殊性,可通过检验铵根的存在而确认溶液为硫酸铵.
解答:解:(1)[实验探究]某温度下饱和溶液的溶质质量分数的值不会大于该温度下溶质的溶解度,常温下硫酸钠的溶解度为19.5g,则常温下它的饱和溶液的溶质的质量分数=
×100%=16.3%<20.0%,因此,该溶液不可能是硫酸钠,故猜想②不成立;
(2)硫酸镁、硫酸、硫酸铵三种物质中只有硫酸镁能与碱溶液氢氧化钠溶液形成氢氧化镁沉淀,因此,观察到出现白色沉淀就可判断溶液为硫酸镁溶液,说明所使用的试剂为氢氧化钠等碱的溶液;由于硫酸溶液、硫酸铵溶液都呈酸性的原因,测出溶液的pH小于7时,并不能就断定溶液为硫酸溶液,也可能是硫酸铵溶液;
(3)只要检验出溶液中含有铵根离子即可说明溶液为硫酸铵,因此可取溶液加入少量氢氧化钠溶液并微热,在试管口放一张湿润的红色石蕊试纸,观察到有刺激性气味气体产生、试纸变成蓝色,即可说明溶液中含有铵根离子,可确认溶液为硫酸铵溶液.所以填表如下:
故答案为:(1)常温下Na2SO4溶液的溶质质量分数不可能达到20%.(2)①NaOH,结论不正确,(NH4)2SO4溶液也呈酸性;(3)见上表.
| 19.5g |
| 100g+19.5g |
(2)硫酸镁、硫酸、硫酸铵三种物质中只有硫酸镁能与碱溶液氢氧化钠溶液形成氢氧化镁沉淀,因此,观察到出现白色沉淀就可判断溶液为硫酸镁溶液,说明所使用的试剂为氢氧化钠等碱的溶液;由于硫酸溶液、硫酸铵溶液都呈酸性的原因,测出溶液的pH小于7时,并不能就断定溶液为硫酸溶液,也可能是硫酸铵溶液;
(3)只要检验出溶液中含有铵根离子即可说明溶液为硫酸铵,因此可取溶液加入少量氢氧化钠溶液并微热,在试管口放一张湿润的红色石蕊试纸,观察到有刺激性气味气体产生、试纸变成蓝色,即可说明溶液中含有铵根离子,可确认溶液为硫酸铵溶液.所以填表如下:
| 实验操作 | 实验现象 | 实验结论 | ||||
| 向试管中加入少量NaOH溶液并加热,将湿润的红色石蕊试纸放在试管口 | 有刺激性气味的气体产生, 红色石蕊试纸变蓝 | (NH4)2SO4+2NaOH
|
点评:本题涉及基础知识和技能较多,熟练掌握饱和溶液溶质质量分数与溶解度的关系、铵根的检验、溶液酸碱性与pH关系等知识,是解答本题的基础.

练习册系列答案
相关题目