题目内容
11.老师在讲台上做氧化钙与水反应的实验.将水加到氧化钙中后,同学们都看到有白色烟雾状物质生成,生成的是什么物质?下面请你就这一问题进行探究:
(1)你猜测生成的物质是什么?至少写出两种:可能是水蒸气液化成的小水滴或也可能是随热气飘出的氢氧化钙固体小颗粒,或两者都有.
(2)“为什么烟雾还会在空气中上升呢?”有同学又提出了问题.你能解释白色烟雾在空气中上升的原因吗?由于氧化钙与水反应放热,放出的热使其上方的空气被加热,体积膨胀,密度变小,气团上升.
(3)你如何通过实验来证明你在(1)中所做猜测的合理性呢?简要写出实验用品反应时,在其上方罩一干净的玻璃片.若玻璃片上有液滴出现,则可说明上升的是小水滴;
若玻璃片上有粉末出现,将粉末湿润后用pH试纸检验,呈碱性,则说明上升的是固体小颗粒:若两种现象均有,则说明上升的烟雾中既有小水滴又有氢氧化钙小颗粒.
分析 (1)氧化钙遇水反应生成氢氧化钙,反应放出大量的热;剧烈反应时放出的大量的热使水变成水蒸气,氢氧化钙为白色粉末也会随水蒸气飘浮形成白色烟雾;
(2)在空气中上升的现象可说明烟雾受到浮力大于自身的重量,烟雾与周围空气混在一起形成气团,气团中空气受热体积膨胀密度减小而使所受浮力增大而导致上升;
(3)可利用烧杯收集烟雾,并根据氢氧化钙溶于水所得溶液呈碱性,能使无色酚酞试液变成红色,检验收集到的粉末.
解答 解:(1)根据氢化钙与水反应只会生成氢氧化钙,因此,猜测烟雾为氢氧化钙的烟粉末或是受热而蒸发的水蒸气或是两者的混合物质;故答案为:可能是水蒸气;也可能是随热气飘出的氢氧化钙固体小颗粒或两者都有;
(2)氧化钙与水剧烈反应放出的大量的热不能及时扩散,导致周围空气受热而迅速膨胀,膨胀后的空气上升而带动烟雾随之上升;故答案为:由于氧化钙与水反应热使其上方的空气被加热,体积膨胀,密度变小,气团上升;
(3)可采取在反应时罩一干净的烧杯,把产生的烟雾进行收集;若杯壁有水滴,说明烟雾含有水;若杯壁为白色粉末,把粉末溶解后滴加酚酞变红时,可判断粉末为氢氧化钙;若既有水滴又有粉末,可以说明烟雾为二者的混合物;故答案为:反应时,在其上方罩一干净的小烧杯,若有水珠,则说明是小水滴;若杯壁有粉末出现,将粉末加水溶解后加入酚酞,变红则证明是氢氧化钙固体小颗粒,若两种现象都有则证明既有水蒸气也有氢氧化钙固体小颗粒.
答案:
(1)可能是水蒸气液化成的小水滴,也可能是随热气飘出的氢氧化钙固体小颗粒,或两者都有
(2)由于氧化钙与水反应放热,放出的热使其上方的空气被加热,体积膨胀,密度变小,气团上升.
(3)反应时,在其上方罩一干净的玻璃片.若玻璃片上有液滴出现,则可说明上升的是小水滴;
若玻璃片上有粉末出现,将粉末湿润后用pH试纸检验,呈碱性,则说明上升的是固体小颗粒:若两种现象均有,则说明上升的烟雾中既有小水滴又有氢氧化钙小颗粒
点评 根据反应或变化规律的特点,对反应后所得物质进行猜测时,借助质量守恒思想对反应后所得物质进行大胆猜测;并用检验猜想.

 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案| 化学反应 | 化学方程式 | 简答 |
| 铁丝在纯氧中燃烧 | 生成物的颜色为黑色 | |
| 红磷燃烧 | 反应物的物质的量之比为4:5. | |
| 硫酸铜溶液中加入氢氧化钠溶液 | 现象:产生蓝色沉淀 | |
| 硫在氧气中燃烧 | 生成物会引起的一种环境问题是形成酸雨 |
【提出问题】在平时探讨酸的性质时,我们通常是讨论酸的水溶液.究竟水在酸显示酸的特性时扮演什么角色呢?
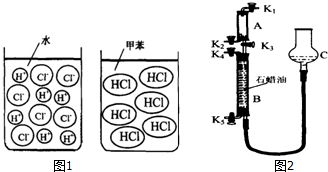
【确定研究对象】以我们最熟知的盐酸(氯化氢的水溶液)和氯化氢进行探究.
【查阅资料】氯化氢溶于水时解离出氢离子和氯离子,而溶于干燥的甲苯(一种有机溶剂)时仍以氯化氢分子的形式分散(如图1).
【设计与实验】(请完成下表)
| 实验内容 | 实验现象 | 解释与结论 |
| 测定导电性 | 氯化氢的水溶液:导电性良好 | 氯化氢的水溶液中有自由移动的离子 |
| 氯化氢的甲苯溶液:不导电 | 氯化氢的甲苯溶液没有自由移动的离子 | |
| 与镁作用 | 氯化氢的水溶液:有气泡产生 | 化学方程式: Mg+2HCl═MgCl2+H2↑ |
| 氯化氢的甲苯溶液:没有明显现象 | 氯化氢的甲苯溶液没有解离出氢离子 | |
| 与固态碳酸钠作用 | 氯化氢的水溶液:产生气泡 | 化学方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑ |
| 氯化氢的甲苯溶液:没有气泡产生 | 氯化氢的甲苯溶液没有解离出氢离子 |
水对酸显现其酸性性质非常重要.还有哪些实例或实验也可以体现水对酸显现其酸性性质的重要性呢,是否没有水,酸就不能显现酸性性质呢?(此问不作答,请在今后的学习中继续关注.)
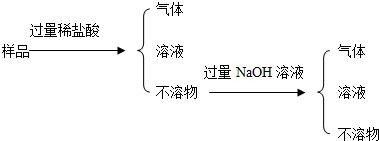
【拓展探究】该学习小组又尝试用图2所示装置进行氯化氢气体与氨气反应的实验探究,活塞K1、K2、K3、K4、K5均关闭(装置气密性好).通过调节活塞,用排石蜡油的方法在B管中收集满了氨气.通过调节活塞K1、K2、K3,在干燥的A管中充入与大气压强相等的干燥氯化氢气体,其操作是打开K1、K2,与K2处导管口连接并通入干燥的HCl气体,集满后,先关闭K2,再关闭K1.在不用任何试剂的情况下,当看到K1导管口处有大量白雾出现现象时,说明A管中已收集满了氯化氢气体.打开K3,氯化氢气体与氨气发生化合反应,生成一种铵盐,写出反应的化学方程式:NH3+HCl=NH4Cl•
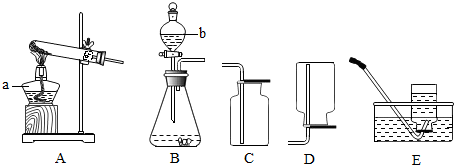
(已知:Si+2NaOH+H2O═Na2SiO3+2H2↑ )
由此可推知,硬铝的组成可能为( )
| A. | Al Cu Mg Si | B. | Al Mg Si Zn | ||
| C. | Al Fe C Cu | D. | Al Mg Zn Fe |
| A. | H2 | B. | H | C. | 2H | D. | H2O |
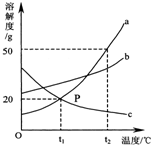 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答: