题目内容
8.化学就在我们身边.请根据所学化学知识回答下列问题:(1)在AgNO3、Cu(NO3)2的混合溶液中加入一定量锌粉,充分反应后过滤,得滤渣和滤液.
①若滤液呈无色,则滤渣中一定含有的物质是Ag,Cu(填化学式);
②若向滤渣中滴加稀盐酸,无明显现象,则滤液中所含溶质的成分可能有三种情况.
(2)工业上可用一氧化碳还原赤铁矿(主要成分是Fe2O3)炼铁,请用化学方程式表示Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
分析 (1)据金属活动性由强到弱的顺序为锌>氢>铜>银,向滤出的固体中加入稀盐酸,有气泡冒出,说明了固体中含锌,可判断加入锌粉过量.
(2)根据炼铁的原理写出反应的化学方程式.
解答 解:(1)①根据金属活动性由强到弱的顺序为锌>氢>铜>银,向溶液中加入一定量的锌粉,根据优先原则,锌先与硝酸银溶液反应生成银和硝酸锌,当硝酸银完全反应完之后锌才能与硝酸铜反应生成铜和硝酸锌,滤液呈无色,说明铜被完全置换,则银早已置换出来,则滤渣中一定含有的物质是银和铜;故填:Ag,Cu;
②若向滤渣中滴加稀盐酸,无明显现象,则滤液中一定没有硝酸银,可能是硝酸锌、硝酸铜、硝酸锌与硝酸铜;故填:三;
(2)一氧化碳和氧化铁在高温时会反应生成铁和二氧化碳,反应的方程式是:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;故填:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
故答案为:
(1)①Ag,Cu; ②三; (2)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
点评 活动性强的金属放入活动性弱的金属的混合盐溶液中,活动性强的金属会先把活动性最弱的金属从其盐溶液中置换出来,然后再置换活动性较弱的金属.

练习册系列答案
相关题目
18.某同学想用实验证明CuSO4溶液显蓝色是由Cu2+造成的,下列实验无意义的是( )
| A. | 将CuSO4溶液加水稀释 | B. | 观察Cu( NO3)2溶液 | ||
| C. | 观察Na2SO4 | D. | 向CuSO4溶液中滴加足量NaOH溶液 |
19.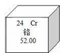 元素周期表是学习化学的重要工具,如图是元素周期表中的一格,下面从该图获取的信息中,正确的 是( )
元素周期表是学习化学的重要工具,如图是元素周期表中的一格,下面从该图获取的信息中,正确的 是( )
 元素周期表是学习化学的重要工具,如图是元素周期表中的一格,下面从该图获取的信息中,正确的 是( )
元素周期表是学习化学的重要工具,如图是元素周期表中的一格,下面从该图获取的信息中,正确的 是( )| A. | 该元素相对原子质量为 52kg | B. | 该元素属于非金属元素 | ||
| C. | 该元素的原子核外有 24 个电子 | D. | 该元素的原子序数为 52 |
16.下列说法正确的是( )
| A. | 当可燃物的温度达到着火点时,就发生燃烧 | |
| B. | 燃着的酒精灯被碰倒,引发酒精在桌面燃烧,可用湿布盖灭 | |
| C. | 二氧化碳能用于灭火是因为二氧化碳的密度比空气的密度大 | |
| D. | 将木柴架空燃烧会更旺,原因是这样能提高空气中氧气的含量 |
3.如图所示的实验操作中,正确的是( )
| A. | 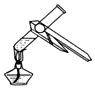 给液体加热 | B. |  放入铁钉 | ||
| C. | 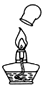 用灯帽熄灭酒精的 | D. | 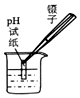 测溶液的酸碱度 |
13.下列质量增加的变化有一种与其他三种存在着本质的区别,这种变化是( )
| A. | 长期放置在空气中的氢氧化钠质量增加 | |
| B. | 久置在潮湿空气中的铁钉质量增加 | |
| C. | 长期敞口放置的浓硫酸质量增加 | |
| D. | 久置在空气中的生石灰质量增加 |
20.如表除杂(括号内为杂质)设计,所选试剂和操作方法均正确的是( )
| 选项 | 物质 | 所选试剂 | 操作方法 |
| A | HCl气体(H2O) | 固体氢氧化钠 | 通过装有试剂的干燥管,收集 |
| B | CaCl2溶液(HCl) | 碳酸钙粉末 | 加过量试剂,充分反应,过滤 |
| C | KNO3溶液(CuSO4) | Ba(OH)2溶液 | 加过量试剂,充分反应,过滤 |
| D | CaCO3固体(CaCl2) | 水 | 加过量试剂,溶解、过滤、洗涤干燥 |
| A. | A | B. | B | C. | C | D. | D |
17.有一Fe和FeO的混合物,测得其中铁元素的质量分数为80%,取该混合物7.0g,加足量稀硫酸完全溶解,生成硫酸亚铁的质量为( )
| A. | 7.6g | B. | 15.2g | C. | 20.0g | D. | 40.0g |
18.向含有AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,若有气泡产生,则下列说法正确的是( )
| A. | 滤出的固体是Ag、Cu两种单质的混合物 | |
| B. | 滤出的固体中一定有铜,可能有银 | |
| C. | 滤液中的离子种类为2种 | |
| D. | 滤液中还有1种溶质 |