题目内容
17.化学就在我们身边,它与我们的生活息息相关.(1)现有H、C、O、Na四种常见的元素,请选用其中的元素写出符合下列要求的物质各一种(用化学式表示):
①供给呼吸的气体O2;②食醋中的酸CH3COOH;
③炉具清洁剂中的碱NaOH;④汽水中溶解的气体CO2.
(2)请回答下列问题:
①日常生活中的自来水属于混合物(填“纯净物”或“混合物”); 自来水中的游离氯有少量可转变成氯离子,氯离子的符号是Cl-.
②四月是鲜花盛开的季节,漫步在花丛中,会闻到花香,请用分子的观点解释闻到香味的原因分子不断在运动.
③在普通汽油中加入适量的燃料乙醇可制得乙醇汽油,用乙醇汽油作为汽车燃料越来越普遍.请你答出使用乙醇汽油的优点(一条即可)节省石油资源.
分析 (1)首先根据题意确定物质的化学名称,然后根据题目所提供的元素、书写化学式的方法和步骤写出物质的化学式即可;
(2)①根据物质的组成和离子符号的写法来分析;②根据分子的特征来分析;③根据使用乙醇汽油可以节省石油能源、减少空气污染、促进农业发展等方面分析优点
解答 解:(1)①氧气能供给呼吸,故填:O2;
②食醋是醋酸的水溶液,故填:CH3COOH;
③炉具清洗剂中含有的碱是氢氧化钠,故填:NaOH;
④汽水中溶解有二氧化碳,故填:CO2;
(2)①自来水中含有可溶性杂质,属于混合物,离子符号的书写方法是在元素符号的右上方写出所带的电荷及电性,所以,氯离子的符号为:Cl-.故答案为:混合物;Cl-;
②由于分子是不断运动的,花香的微粒通过运动而花香四溢;故答案为:分子不断在运动;
③使用乙醇汽油可以节省石油资源,减少汽车尾气污染或乙醇属于可再生资源或促进农业生产等.故答案为:节省石油资源.
点评 本题所考查的知识与生活联系比较紧密.学会利用化学知识来解决生活中的一些问题的方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.化学知识中有很多的“相等”.下列叙述正确的是( )
| A. | 原子中原子核内的质子数和中子数一定相等 | |
| B. | 溶液稀释前后溶质的质量一定相等 | |
| C. | 同种元素的原子和离子(如钠原子和钠离子)核外电子数相等 | |
| D. | 一种溶液和一种固体反应,反应后溶液的质量和参加反应的物质的总质量一定相等 |
5.下列图象不能正确反映对应变化关系的是( )
| A. | 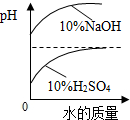 稀释10%NaOH和10% H2SO4 | |
| B. | 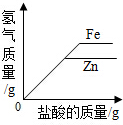 向相等质量锌粉和铁粉中分别加入相同的稀盐酸 | |
| C. | 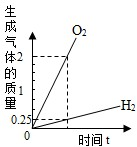 将水通电电解一段时间 | |
| D. | 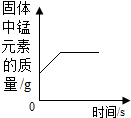 加热一定量高锰酸钾固体 |
2.人类的生产生活离不开金属,下列三种金属被发现、使用的先后顺序依次为铜、铁、铝.
(1)金属大规模被使用的先后顺序跟③(填序号)选项关系最大.
①地壳中金属元衷的含量 ②金属的导电性 ③金属的活动性
(2)为探究锰与铁的金属活动性,在相同温度下,取大小相同的两种金属薄片,用砂纸将表面擦光亮,分别投入等体积、等溶质质量分数的足量稀盐酸中反应,观察现象.请分析回答下列问题:
①两种金属投入盐酸前用砂纸将表面擦光亮,其主要目的是A.
A.除去氧化膜,便于直接反应 B.使表面不平整,易反应
C.表面光亮,易观察 D.提高金属温度,加快反应速度
②根据下表中的现象填写结论.
③除了比较与酸反应产生气体速率的快慢,你还有其他化学方法可比较这两种金属恬动性强弱吗?请举出一种方法(写出原理即可)FeSO4、Mn.
(3)将盛有等质量、等溶质质量分数的稀盐酸的两只烧杯,放在托盘天平左右两盘上,调节至平衡,再向两只烧杯中分别放入质量相等的镁和铁,待反应停止后,请判断:
①若天平仍保持平衡,烧杯中一定没有剩余的物质是稀盐酸.
②若天平失去平衡,则指针一定偏向放铁的一边.
(1)金属大规模被使用的先后顺序跟③(填序号)选项关系最大.
①地壳中金属元衷的含量 ②金属的导电性 ③金属的活动性
(2)为探究锰与铁的金属活动性,在相同温度下,取大小相同的两种金属薄片,用砂纸将表面擦光亮,分别投入等体积、等溶质质量分数的足量稀盐酸中反应,观察现象.请分析回答下列问题:
①两种金属投入盐酸前用砂纸将表面擦光亮,其主要目的是A.
A.除去氧化膜,便于直接反应 B.使表面不平整,易反应
C.表面光亮,易观察 D.提高金属温度,加快反应速度
②根据下表中的现象填写结论.
| 金属 | 铁 | 锰 |
| 与盐酸反应现象 | 放出气泡速度缓慢 | 放出气泡速度较快 |
| 结论 | 锰的金属活泼性大于铁. | |
(3)将盛有等质量、等溶质质量分数的稀盐酸的两只烧杯,放在托盘天平左右两盘上,调节至平衡,再向两只烧杯中分别放入质量相等的镁和铁,待反应停止后,请判断:
①若天平仍保持平衡,烧杯中一定没有剩余的物质是稀盐酸.
②若天平失去平衡,则指针一定偏向放铁的一边.
19.在化学实验室,某小组同学实验时发现一瓶没有密封好的NaOH已经结块.于是对其成分进行科学探究,请你一起完成探究的过程.
Ⅰ固体的成分分析
【提出问题】结块后的固体成分是什么?
【猜想与假设】
猜想一:固体为碳酸钠
猜想二:固体为碳酸钠和氢氧化钠.
用化学方程式表示固体中有碳酸钠的原因CO2+2NaOH═Na2CO3+H2O.
【查阅资料】BaCl2溶液pH=7
【实验探究】从瓶中取出一定量的固体,加入足量水溶解,再将溶液分三等份分别装入A、B、C三支试管,进行如图1所示实验.

甲同学根据实验现象,认为结块固体中有碳酸钠和氢氧化钠.
【实验分析】
(1)根据甲同学的实验结论可知,三支试管中观察到的实验现象分别为:A试管中溶液变红,B试管出现大量气泡,C试管中出现白色沉淀;C试管中现象产生的原因是(用化学方程式表示)Na2CO3+BaCl2=BaCO3↓+2NaCl.
(2)乙同学认为甲同学的结论是不正确的,原因是碳酸钠溶液呈碱性,也是无色酚酞变红.
【实验设计】请你设计合理的实验方案,填入下列表格中.
Ⅱ固体中各成分含量
为确定该固体样品中Na2CO3的质量分数,小芳同学称取2g样品,利用A为Y形管、B为量气管、C为水准管作为主要反应容器,进行了如图2(I)所示实验.
(1)在量气管内水面上架一薄层油,目的是防止二氧化碳溶于水;将Y形管(装置A)向左倾斜,硫酸流到样品中.
(2)使样品与稀硫酸反应的操作为将Y形管(装置A)向左倾斜,硫酸流到样品中.
(3)实验结束后,小芳同学读出量气管中的气体体积为22.4mL(已知该温度压强下,CO2的密度为1.965g/L),请你计算出样品中Na2CO3质量分数.(写出计算过程)
(4)小明同学设计如图2(Ⅱ)装置,分别测定反应前、反应后仪器以及仪器内物质的总质量,进行有关计算,实验操作中没有失误,多次测量的结果均偏大,你认为可能的原因是逸出的二氧化碳中含有水蒸汽.
Ⅰ固体的成分分析
【提出问题】结块后的固体成分是什么?
【猜想与假设】
猜想一:固体为碳酸钠
猜想二:固体为碳酸钠和氢氧化钠.
用化学方程式表示固体中有碳酸钠的原因CO2+2NaOH═Na2CO3+H2O.
【查阅资料】BaCl2溶液pH=7
【实验探究】从瓶中取出一定量的固体,加入足量水溶解,再将溶液分三等份分别装入A、B、C三支试管,进行如图1所示实验.

甲同学根据实验现象,认为结块固体中有碳酸钠和氢氧化钠.
【实验分析】
(1)根据甲同学的实验结论可知,三支试管中观察到的实验现象分别为:A试管中溶液变红,B试管出现大量气泡,C试管中出现白色沉淀;C试管中现象产生的原因是(用化学方程式表示)Na2CO3+BaCl2=BaCO3↓+2NaCl.
(2)乙同学认为甲同学的结论是不正确的,原因是碳酸钠溶液呈碱性,也是无色酚酞变红.
【实验设计】请你设计合理的实验方案,填入下列表格中.
| 操作 | 现象 | 结论 |
| 取少量结块固体于试管(或烧杯)中,加水使其完全溶解,加入过量的氯化钡或氯化钙溶液,静置后,向上层清液(或过滤后向滤液)中滴加几滴无色酚酞溶液 | 若溶液变红 | 固体为碳酸钠和氢氧化钠 |
为确定该固体样品中Na2CO3的质量分数,小芳同学称取2g样品,利用A为Y形管、B为量气管、C为水准管作为主要反应容器,进行了如图2(I)所示实验.
(1)在量气管内水面上架一薄层油,目的是防止二氧化碳溶于水;将Y形管(装置A)向左倾斜,硫酸流到样品中.
(2)使样品与稀硫酸反应的操作为将Y形管(装置A)向左倾斜,硫酸流到样品中.
(3)实验结束后,小芳同学读出量气管中的气体体积为22.4mL(已知该温度压强下,CO2的密度为1.965g/L),请你计算出样品中Na2CO3质量分数.(写出计算过程)
(4)小明同学设计如图2(Ⅱ)装置,分别测定反应前、反应后仪器以及仪器内物质的总质量,进行有关计算,实验操作中没有失误,多次测量的结果均偏大,你认为可能的原因是逸出的二氧化碳中含有水蒸汽.
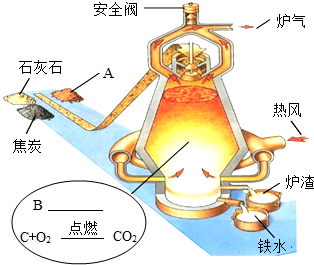 如图是炼铁高炉示意图,请写出物质A的名称铁矿石,B处的反应方程式为CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO,3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;该高炉中最终的产品为生铁.
如图是炼铁高炉示意图,请写出物质A的名称铁矿石,B处的反应方程式为CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO,3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;该高炉中最终的产品为生铁.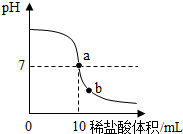 在一堂化学实验课上,老师为每组同学分别提供了一瓶氢氧化钠溶液,让他们用1%的稀盐酸来测定其溶质的质量分数.以下是几组同学的设想及做法:
在一堂化学实验课上,老师为每组同学分别提供了一瓶氢氧化钠溶液,让他们用1%的稀盐酸来测定其溶质的质量分数.以下是几组同学的设想及做法: