题目内容
18.善于归纳知识,有利于提高自身能力.下列知识整理的内容不完全正确的一组是( )| A.物质的分类 | B.化学与生活 |
| ①单质是只含一种元素的纯净物 ②含有氧元素的化合物不一定是氧化物 | ①干冰-用于人工降雨 ②除去餐具油污-用洗洁精乳化 |
| C.化学实验数据记录 | D.化学中常见的“三” |
| ①用托盘天平称取0.56g铁粉 ②用10mL量筒量取7.25mL水 | ①工业三废-废渣、废水、废气 ②三大合成材料-塑料、合成纤维、合成橡胶 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.根据单质与氧化物的概念来分析;
B.根据物质的性质与用途来分析;
C.根据仪器的精确度与记录方法来分析;
D.根据工业三废与三大合成材料来分析.
解答 解:A.由一种元素组成的纯净物属于单质;氧化物是由两种元素组成的化合物,其中有一种元素是氧元素,但是含有氧元素的化合物不一定属于氧化物,如氯酸钾,故正确;
B.干冰易升华吸热,可用于人工降雨;洗洁精有乳化作用,可用来除去油污,故正确;
C.托盘天平只能精确到0.1g;量筒能精确到0.1mL,故错误;
D.工业三废是指:废渣、废水、废气;三大合成材料是指:塑料、合成纤维、合成橡胶,故正确.
故选C.
点评 本题主要考查物质的性质和用途,解答时要充分理解各种物质的性质,然后再根据物质的性质方面进行分析、判断,从而确定物质的用途.

练习册系列答案
相关题目
9.火箭使用的一种燃料是偏二甲肼,其化学式为C2H8N2,燃烧时发生如下反应:C2H8N2+2X $\frac{\underline{\;点燃\;}}{\;}$ 2CO2+4H2O+3N2,则x的化学式为( )
| A. | NO | B. | NO2 | C. | N2O | D. | N2O4 |
6.已知一个SO2分子的质量为n千克,一个SO3分子的质量为m千克(假设两种分子中都具有相同硫原子和氧原子).若以一个硫原子质量的$\frac{1}{32}$作为标准,可计算出SO2的式量为( )
| A. | $\frac{32n}{(m-n)}$ | B. | $\frac{32n}{(3m-2n)}$ | C. | $\frac{32n}{(3n-2m)}$ | D. | $\frac{16n}{(3m-2n)}$ |
13.探究小组为了测定某硫酸厂的废水中硫酸的含量,进行了如下实验(假设废水中溶质只含有硫酸)
①取无色澄淸的废水100.0 g于烧杯中.
②向其中逐滴加入质量分数为0.4%的氢氧化钠溶液,用玻璃榉不断搅拌,并用pH计测定反应过程中溶液pH的变化.数据如表所示:
综合以上信息,请回答下列问题:
(1)当废水恰好呈中性时,NaOH溶液累计加入量是200.0g.
(2)计算废水中硫酸的质量分数.(写出计算过程)
①取无色澄淸的废水100.0 g于烧杯中.
②向其中逐滴加入质量分数为0.4%的氢氧化钠溶液,用玻璃榉不断搅拌,并用pH计测定反应过程中溶液pH的变化.数据如表所示:
| 实验次数 | 1 | 2 | 3 | 4 | 5 |
| NaOH溶液累计加入量/g | 0.0 | 50.0 | 100.0 | 150.0 | 200.0 |
| 废水的pH | 5.0 | 5.5 | 6.0 | 6.5 | 7.0 |
(1)当废水恰好呈中性时,NaOH溶液累计加入量是200.0g.
(2)计算废水中硫酸的质量分数.(写出计算过程)
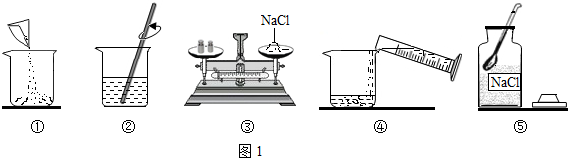
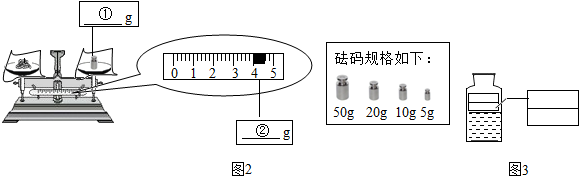
10.观察如图,有关说法正确的是( )


| A. | 图中常见的A、B、C实验基本操作均正确 | |
| B. | 实验室用KMnO4制备O2选用的仪器有D、E、G | |
| C. | 用大理石与稀盐酸制备CO2并使反应随时发生或停止,可选用仪器E和I | |
| D. | 图H、I中相同的仪器有长颈漏斗和玻璃导管 |
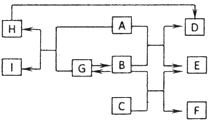 如图所示,A-I都是初中常见的物质,其中D是最清洁的能源,G和F都是红色固体,E和I含有元素的种类相同(箭头表示转化关系,部分反应物省略).回答下列问题
如图所示,A-I都是初中常见的物质,其中D是最清洁的能源,G和F都是红色固体,E和I含有元素的种类相同(箭头表示转化关系,部分反应物省略).回答下列问题