题目内容
16. 如图是电解水的简易装置.回答下列问题:
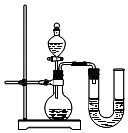
如图是电解水的简易装置.回答下列问题:(1)电解水实验所用到的电源是直流电,则甲管生成氢气(选 填“氧气”或“氢气”)气体,b应接电源正极(选填“正”或“负”).
(2)检验乙管中气体的方法是用带火星的木条检验,木条复燃.
(3)在实际操作时,常在水中滴加少量稀硫酸和氢氧化钠溶液,这是为了增强水的导电性.
(4)理论上甲、乙两试管中气体的体积比为2:1.
(5)通过以上实验得出的结论是水是由氢元素和氧元素组成的.
分析 (1)根据电解水实验的现象、结论分析回答;
(2)根据氧气的性质分析检验的方法;
(3)根据稀硫酸和氢氧化钠在溶于水时能解离出自由移动的离子分析回答;
(4)根据电解水实验的现象回答;
(5)根据水是由氢元素和氧元素组成的解答.
解答 解:(1)由电解水的装置可知,甲管生成的气体较多是氢气,乙管生成的气体较少是氧气,应接电源的正极,所以,b应接电源的正极;
(2)由于乙管中的气体是氧气能支持燃烧,所以,检验的方法是:将带火星的木条伸入试管内看是否复燃;
(3)由于稀硫酸和氢氧化钠在溶于水时能解离出自由移动的离子.所以,在实际操作时,常在水中滴加少量稀硫酸和氢氧化钠溶液,这是为了增强水的导电性;
(4)理论上甲、乙两试管中气体的体积比为2:1;
(5)水通电生成 氢气和氧气,说明水是由氢元素和氧元素组成的.
答案:
(1)氢气;正;
(2)用带火星的木条检验,木条复燃;
(3)增强水的导电性;
(4)2:1;
(5)氢元素和氧元素;
点评 熟练掌握电解水的实验,熟记其反应现象和结论,然后根据现象能够判断电池的正极和负极,记住六个字“正氧一,负氢二”.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.下列实验过程中与图象描述相符的一组是( )
| A. |  两份等质量、等溶质质量分数的双氧水溶液在有无MnO2的情况下产生 | |
| B. |  向等质量的镁、锌中分别加入稀盐酸 | |
| C. |  向一定质量的稀盐酸和氯化铜的混合溶液中加入氢氧化钠溶液 | |
| D. |  室温下,向一定质量的饱和石灰水中加入氧化钙 |
11.下列说法正确的是( )
| A. | 一个水分子是由两个氢气和一个氧气构成的 | |
| B. | 一个水分子是由两个氢元素和一个氧元素组成的 | |
| C. | 一个水分子是由两个氢原子和一个氧原子组成的 | |
| D. | 一个水分子是由两个氢原子和一个氧原子构成的 |
1.请根据下表回答有关问题.
(1)榔芋皮上含有一种碱性的物质--皂角素,皮肤沾上它会奇痒难忍,你认为可选用上表中①来涂抹止痒.(用序号填写)
(2)用表中的物质作为反应物,写出制取氢氧化钠的化学方程式:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
| 序号 | ① | ② | ③ | ④ |
| 物质 | 醋酸 | 高锰酸钾 | 熟石灰 | 纯碱 |
| 化学式 | CH3COOH | KMnO4 | Ca(OH)2 | Na2CO3 |
(2)用表中的物质作为反应物,写出制取氢氧化钠的化学方程式:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
5. 某兴趣小组为证明氢氧化钠溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.
某兴趣小组为证明氢氧化钠溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.
方案一:先在氢氧化钠溶液中滴加几滴酚酞试液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明氢氧化钠溶液与稀盐酸发生了化学反应.该组同学在向氢氧化钠溶液中滴加酚酞试液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞试液,溶液逐渐变成了红色,过了一会儿红色就消失了.该小组同学对这种意外现象的原因做了如下猜想:
①可能是酚酞试液与空气中的氧气反应,使红色消失;
②可能是酚酞试液与空气中的二氧化碳反应,使红色消失.
(1)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴入酚酞试液.实验中是“滴入植物油”的目的是隔绝氧气.
实验结果证明酚酞试液红色消失与空气中的氧气无关.
(2)为验证猜想②,该组同学做了如下实验:取一定量的碳酸钠溶液,在其中滴入酚酞试液,发现溶液也呈红色,由此可以得出以下两个结论:
结论1:说明碳酸钠溶液呈碱性;
结论2:说明酚酞试液红色消失与空气中的二氧化碳无关.
(3)该小组同学通过查阅资料得知:当氢氧化钠溶液浓度很大时,就会出现上述意外现象.设计实验证明该方案中取用的氢氧化钠溶液浓度过大:
实验方法:
①取上述氢氧化钠溶液分为AB两等份
②B溶液中加足量的水稀释
③分别滴加等量酚酞
观察到的现象A溶液:溶液变成红色且过一会后红色消失
B溶液:溶液变成红色且过一会后红色不消失
方案三:化学反应中通常伴随能量的变化,可借助反应前后温度的变化判断反应的发生.该组同学将不同浓度的盐酸和氢氧化钠溶液各10mL混合,用温度计测定室温下混合前后溶液温度的变化,并记录了每次混合前后温度的升高值△t(如表).
(4)表中X=7.
(5)某同学在没使用温度计的情况下,通过上图所示装置完成了实验.该同学根据U形管中左边液面下降判断氢氧化钠溶液与稀盐酸发生了中和反应.
 某兴趣小组为证明氢氧化钠溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.
某兴趣小组为证明氢氧化钠溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.方案一:先在氢氧化钠溶液中滴加几滴酚酞试液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明氢氧化钠溶液与稀盐酸发生了化学反应.该组同学在向氢氧化钠溶液中滴加酚酞试液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞试液,溶液逐渐变成了红色,过了一会儿红色就消失了.该小组同学对这种意外现象的原因做了如下猜想:
①可能是酚酞试液与空气中的氧气反应,使红色消失;
②可能是酚酞试液与空气中的二氧化碳反应,使红色消失.
(1)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴入酚酞试液.实验中是“滴入植物油”的目的是隔绝氧气.
实验结果证明酚酞试液红色消失与空气中的氧气无关.
(2)为验证猜想②,该组同学做了如下实验:取一定量的碳酸钠溶液,在其中滴入酚酞试液,发现溶液也呈红色,由此可以得出以下两个结论:
结论1:说明碳酸钠溶液呈碱性;
结论2:说明酚酞试液红色消失与空气中的二氧化碳无关.
(3)该小组同学通过查阅资料得知:当氢氧化钠溶液浓度很大时,就会出现上述意外现象.设计实验证明该方案中取用的氢氧化钠溶液浓度过大:
实验方法:
①取上述氢氧化钠溶液分为AB两等份
②B溶液中加足量的水稀释
③分别滴加等量酚酞
观察到的现象A溶液:溶液变成红色且过一会后红色消失
B溶液:溶液变成红色且过一会后红色不消失
方案三:化学反应中通常伴随能量的变化,可借助反应前后温度的变化判断反应的发生.该组同学将不同浓度的盐酸和氢氧化钠溶液各10mL混合,用温度计测定室温下混合前后溶液温度的变化,并记录了每次混合前后温度的升高值△t(如表).
| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | X |
| 3 | 7.30% | 8.00% | 1 4 |
(5)某同学在没使用温度计的情况下,通过上图所示装置完成了实验.该同学根据U形管中左边液面下降判断氢氧化钠溶液与稀盐酸发生了中和反应.


 某科学兴趣小组利用铜丝、铁丝、FeSO4溶液、CuSO4溶液、AgNO3溶液等实验药品,来探究铁、铜与银三种金属的化学活动性,并设计了如图所示的实验方案:将铁丝与铜丝分别浸入盛有CuSO4溶液和AgNO3溶液的两支试管中,观察实验现象.试回答下列问题:
某科学兴趣小组利用铜丝、铁丝、FeSO4溶液、CuSO4溶液、AgNO3溶液等实验药品,来探究铁、铜与银三种金属的化学活动性,并设计了如图所示的实验方案:将铁丝与铜丝分别浸入盛有CuSO4溶液和AgNO3溶液的两支试管中,观察实验现象.试回答下列问题: .
.