题目内容
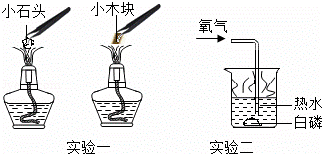
为测定一瓶失去标签的过氧化氢溶液的溶质质量分数,某同学取50.0g过氧化氢溶液放入烧杯中,然后加入2.0g二氧化锰,等不再放出气体,称得烧杯中剩余物质的总质量为50.4g.计算:
(1)过氧化氢中氢元素和氧元素的质量比为 .
(2)此过氧化氢溶液的溶质质量分数.(写出计算过程)
1:16
根据质量守恒定律可以知道,生成氧气的质量是50.0g+2g﹣50.4g=1.6g
设该过氧化氢溶液中溶质的质量为x
2H2O2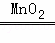 2H2O+O2↑
2H2O+O2↑
68 32
x 1.6g
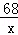 =
= 解得:x=3.4g
解得:x=3.4g
此过氧化氢溶液的溶质质量分数为: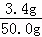 ×100%=6.8%
×100%=6.8%
答:此过氧化氢溶液的溶质质量分数为6.8%.

 天天练口算系列答案
天天练口算系列答案化肥对提高农作物的产量具有重要的作用,碳铵(碳酸氢铵)就是农民朋友经常使用的一种氮肥,碳铵易溶于水、受潮时常温分解,温度越高分解越快,遇碱时放出氨气.某校化学兴趣小组为测定某碳铵肥料样品的纯度,将8.5g样品加入足量的浓氢氧化钠溶液中共热,(碳铵中的杂质不与氢氧化钠反应,反应的方程式为NH4HCO3+2NaOH=Na2CO3+2H2O+NH3↑),把产生的所有NH3用足量的硫酸溶液吸收,同时测量两分钟内硫酸溶液增加的质量,结果如下表所示.
| 时间/S | 0 | 20 | 30 | 40 | 60 | 80 | 100 | 120 |
| 增加质量/g | 0 | 0.7 | m | 1.2 | 1.5 | 1.6 | 1.7 | 1.7 |
试回答下列问题:
(1)根据碳酸氢铵的性质,你认为在使用碳铵肥料时应注意的问题是 .
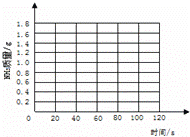
(2)请在如图所示的坐标纸上,以反应时间为横坐标,以产生NH3质量为纵坐标,画出产生气体的质量随时间变化的关系曲线,并判断表中m约为 .
(3)试计算该样品中碳酸氢铵的质量分数(写出计算过程,计算结果保留一位小数).
化学兴趣小组的同学在老师的指导下,开展如下探究活动.
探究一:A、B、C、D分别是纯碱、烧碱、氯化钠、硫酸钠中的一种,它们之间的转化关系如图所示.
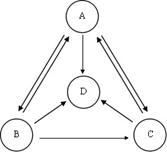
⑴四种物质中,属于碱的是 (填化学式,下同).
⑵物质B是 .
探究二:工业品烧碱含有少量氯化钠杂质。该小组同学从一瓶久置的工业品烧碱样品中取出一定量,在烧杯中加适量水溶解后 得到样品溶液。用稀硫酸与样品溶液做中和反应实验。有关实验操作和现象如下:
得到样品溶液。用稀硫酸与样品溶液做中和反应实验。有关实验操作和现象如下:
| 实验步骤 | 实验现象 |
| Ⅰ向样品溶液中滴加酚酞溶液 | 溶液呈红色 |
| Ⅱ向样品溶液中滴加稀硫酸, 并用玻璃棒 | 滴加一定量稀硫酸后溶液中开始产生气泡 溶液仍呈红色 |
该小组同学对于实验所得红色溶液很感兴趣,展开讨论。溶液里的中和反应是否已经完成?一部分同学认为还没有完成,理由是操作Ⅱ后“溶液仍呈红色”;而另一部分同学则认为中和反应已经完成。结果经过师生共同讨论,确认溶液里中和反应已经完成.
⑶样品溶液的pH 7(填写“<、= 或 >”).
⑷确认溶液里中和反应已经 完成所依据的现象是 .
完成所依据的现象是 .
最后,他们设计一个实验方案,验证了久置的工业品烧碱样品中确实含有氯化钠杂质且已经部分变质,并提纯工业品烧碱。其实验流程及部分实验现象如图所示。
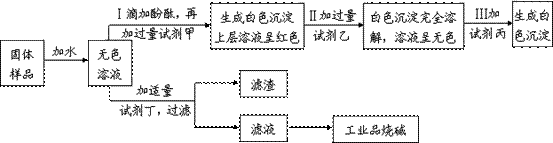
⑸试剂甲和试剂乙的溶液中阴离子都是 (填离子符号).
⑹试剂丁是 (填化学式).
⑺证明工业品烧碱样品已经部分变质的证据是 .
 搅拌
搅拌