题目内容
1.用作牙膏摩擦剂的轻质碳酸钙可以用石灰石(主要成分是碳酸钙)来制备,某化学兴趣小组设计了生产流程,如图所示: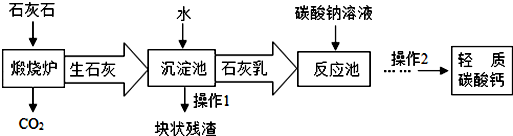
已知:生石灰与水充分反应后可得到颗粒非常细小的熟石灰浆(石灰乳).
(1)在“煅烧炉”中发生反应的化学方程式是CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,该反应类型属于分解反应.
(2)在“沉淀池”中发生反应的化学方程式是Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(3)在反应池中发生的化学反应是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH,若要分离出“反应池”中的沉淀物,流程中“操作2”的名称是过滤.
(4)在工艺流程图中可以用煅烧炉排出的CO2气体替代“碳酸钠溶液”,这样做的优点是原料利用率高,降低生产成本,减少温室气体二氧化碳排放.(任写1点)
分析 (1)根据碳酸钙高温煅烧生成氧化钙和二氧化碳进行分析;
(2)根据碳酸钠与氢氧化钙发生反应生成碳酸钙沉淀和氢氧化钠进行分析;
(3)根据过滤是将不溶于液体的固体分离出来的一种方法进行分析;
(4)根据用二氧化碳代替碳酸钠溶液,可达到降低生产成本和节能减排进行分析.
解答 解:(1)煅烧炉中的反应是:石灰石经高温煅烧生成生石灰和二氧化碳,该反应满足分解反应一变多的条件,属于分解反应,化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;
(2)反应池中的反应是:碳酸钠与氢氧化钙发生反应,生成碳酸钙沉淀和氢氧化钠,其反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(3)过滤是把不溶于溶液的固体和液体分开的一种分离混合物的方法,“反应池”中的混合物分离出生成的碳酸钙固体,可用过滤的方法;
(4)用二氧化碳代替碳酸钠溶液,可达到降低生产成本和节能减排.
故答案为:(1)故答案是:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,分解;
(2)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(3)过滤;
(4)原料利用率高,降低生产成本,减少温室气体CO2排放.
点评 本题主要考查了化学方程式的书写以及悬浊液的定义及过滤的方法,考查较为全面

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
12.已知一个X原子的质量为Mkg,一个标准碳原子质量为Nkg,则X的相对原子质量为( )
| A. | 12MNkg | B. | 12MN | C. | $\frac{12N}{M}$ | D. | $\frac{12M}{N}$ |
9.区分下列各物质,所加试剂或操作方法完全正确的是( )
| 方法1 | 方法2 | |
| A | 看颜色 | 滴加稀盐酸 |
| B | 闻气味 | 通过灼热的氧化铜 |
| C | 测pH | 蒸发结晶 |
| D | 看颜色 | 灼烧 |
| A. | 铁粉和铜粉 | B. | 一氧化碳和二氧化碳 | ||
| C. | 食盐水和蒸馏水 | D. | 真黄金和假黄金(铜锌合金) |
13.把一定质量的纯净物E和40g的纯净物F,按图进行反应.反应结束后,可生成44g G物质和9g H物质.下列关于该反应的说法正确的是( )
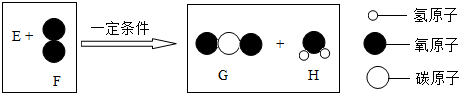

| A. | H中氢元素的质量为2克 | B. | E为含氧化合物 | ||
| C. | G和H的分子个数比为1:2 | D. | E分子中原子个数比为1:1 |