题目内容
1.我国沿海地区素有“夏天晒盐,冬天捞碱”的传统,请简述其原理.分析 根据溶解度受影响的大小,选择结晶的操作方法--蒸发结晶或降温结晶法;溶解度受温度影响不大的物质结晶时一般采取蒸发结晶的方法,溶解度受温度影响较大的物质结晶时一般采取降温结晶的方法.
解答 解:“夏天晒盐”是因为食盐的溶解度受温度变化的影响不大,夏天气温高,水分蒸发快,食盐易结晶析出.
“冬天捞碱”,是因为纯碱的溶解度受温度变化的影响较大,冬天气温低,纯碱易结晶析出.
故答案为:“夏天晒盐”是因为食盐的溶解度受温度变化的影响不大,夏天气温高,水分蒸发快,食盐易结晶析出;
“冬天捞碱”,是因为纯碱的溶解度受温度变化的影响较大,冬天气温低,纯碱易结晶析出.
点评 本题难度不大,掌握结晶的原理(蒸发结晶、降温结晶)、适用范围并能灵活运用是正确解答此类题的关键

练习册系列答案
相关题目
11.下列变化过程中,发生放热的是( )
| A. | 洒在地上的水变干了 | B. | 深秋,屋顶的瓦上结了一层霜 | ||
| C. | 将硝酸铵固体溶于水 | D. | 木炭与二氧化碳高温下发生反应 |
12.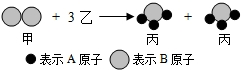 甲分子与乙分子反应生成丙分子的示意图如图所示,下列说法中,不正确的是( )
甲分子与乙分子反应生成丙分子的示意图如图所示,下列说法中,不正确的是( )
 甲分子与乙分子反应生成丙分子的示意图如图所示,下列说法中,不正确的是( )
甲分子与乙分子反应生成丙分子的示意图如图所示,下列说法中,不正确的是( )| A. | 物质乙是单质 | |
| B. | 丙分子中A、B原子个数比为3:1 | |
| C. | 此反应属于化合反应 | |
| D. | 化学反应N2+3H2═2NH3与示意图不相符 |
6.下表列出了除去物质中所含少量杂质的方法,其中错误的是( )
| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | CO | CO2 | 通过足量氢氧化钠溶液,干燥 |
| B | NaCl | CaCO3 | 溶解、过滤、蒸发 |
| C | KOH溶液 | K2CO3 | 加入足量稀盐酸至不再产生气泡 |
| D | FeCl2溶液 | CuCl2 | 加入过量铁粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |
13.大蒜中含有一种有效成分辣素“硫化丙烯”,其化学式为C3H6S,能杀菌,具有一定的抗病功能和食疗价值.下列关于硫化丙烯的说法中正确的是( )
| A. | 硫化丙烯中碳元素的质量分数最大 | |
| B. | 硫化丙烯分子由3个碳原子、6个氢原子、1个硫原子构成 | |
| C. | 硫化丙烯由碳、氢、氧三种元素组成 | |
| D. | 硫化丙烯分子中C、H元素原子质量比为2:1 |
11.如图各项实验操作正确的是( )
| A. | 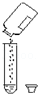 液体药品取用 | B. | 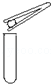 向试管中添加块状固体 | ||
| C. |  取用粉末状药品 | D. | 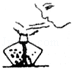 熄灭酒精灯 |
