题目内容
11. 溶液在日常生产生活及科学研究中具有广泛的用途.现实验室需配制一定溶质质量分数的氯化钠溶液.
溶液在日常生产生活及科学研究中具有广泛的用途.现实验室需配制一定溶质质量分数的氯化钠溶液.(1)计算:配制50g质量分数为6%的氯化钠溶液,所需氯化钠的质量为3g;
(2)称量:分别在托盘天平左右两盘放上纸片,调节平衡后,A(填字母编号);
A.先移动游码到所需位置,再添加氯化钠直到天平平衡
B.先添加所需的氯化钠,再移动游码直到天平平衡
(3)量取:量取所需蒸馏水要用到的仪器是量筒、胶头滴管(填仪器名称).
(4)溶解:将称量好的氯化钠和蒸馏水混合溶解,此处玻璃棒的作用是加速溶解.
(5)用已配好的质量分数为6%的氯化钠溶液(密度为1.04g/cm3)配制50g质量分数为3%的氯化钠溶液,所需质量分数为6%的氯化钠溶液体积为24.0mL(计算结果保留到0.1):加水的体积为25mL.
分析 (1)根据溶质质量=溶液质量×溶质质量分数进行分析;
(2)根据利用天平称量一定量物质的质量的步骤分析判断;
(3)根据量取液体需要的仪器是量筒、胶头滴管进行分析;
(4)根据玻璃棒在溶解过程中的作用进行分析;
(5)根据溶液稀释前后的溶质质量不变进行分析.
解答 解:(1)所需氯化钠的质量为:50g×6%=3g;
(2)要称量3g的氯化钠,应分别在天平左右两盘放上纸片,防止药品沾在托盘上,调节平衡后,先移动游码到所需位置,再添加氯化钠直到天平平衡,故选A;
(3)量取液体需要的仪器是量筒、胶头滴管;
(4)玻璃棒在溶解过程中的作用是加速溶解;
(5)设所需氯化钠溶液的体积为x
x×1.04g/cm3×6%=50g×3%
x=24.0mL,
需要水的质量为:50g-24.0mL×1.04g/cm3=25g合25mL.
故答案为:(1)3g;
(2)A;
(3)量筒、胶头滴管;
(4)加速溶解;
(5)24.0mL,25mL.
点评 本题考查知识比较细致、全面,因此同学们要注重平时知识的积累,才能结合选项依据所学知识正确分析和解答.

练习册系列答案
相关题目
1.下列实验操作正确的是( )
| A. |  加热液体 | B. |  稀释浓硫酸 | C. |  检验气密性 | D. |  熄灭酒精灯 |
19.下列实验操作能达到实验目的是( )
| A. | 取少量溶液,滴加无色酚酞溶液验证氯化钠溶液 | |
| B. | 将铁丝浸入硫酸铜溶液和硝酸银溶液比较铁、铜、银三种金属的金属活动性 | |
| C. | 将铁制品长时间浸没在稀硫酸中以除去铁制品表面的铁锈 | |
| D. | 将粗盐研碎、溶解、过滤、蒸发以除去粗盐中的难溶性杂质 |
6.20℃时,将等质量不含结晶水的甲、乙固体分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2(不考虑水分蒸发),甲、乙固体的溶解度曲线如图3,下列说法错误的是( )
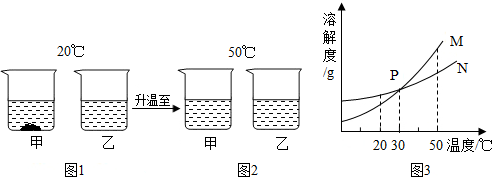

| A. | 图1中,乙一定是饱和溶液 | |
| B. | 图2中,两溶液中溶质的质量分数一定相等 | |
| C. | 图3中,M表示甲的溶解度曲线 | |
| D. | 图2中,两溶液降温至30℃一定都不会析出晶体 |
16.下列实验方法正确的是( )
| A. | 用带火星木条鉴别氮气和空气 | |
| B. | 用紫色石蕊溶液鉴别二氧化碳和一氧化碳 | |
| C. | 用稀硫酸除去铁粉中混有的少量铜粉 | |
| D. | 用稀盐酸除去氧化钙中混有的少量碳酸钙 |
20.物质的用途主要由其性质决定的.下列物质的用途与性质对应不正确的是( )
| A. | 常用氮气做填充保护气--氮气化学性质稳定 | |
| B. | 氧气用于炼钢--支持燃烧 | |
| C. | 干冰做致冷剂保存食物--干冰升华吸热 | |
| D. | 铝制炊具比铁制炊具更耐锈蚀--铝的活动性比铁弱 |
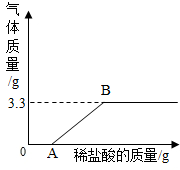 热水瓶用久后,瓶胆内壁常附着一层水垢(主要成分是CaCO3和Mg(OH))2,其它成份忽略不计).某兴趣小组的同学为了探究水垢中Mg(OH)2的含量,取10g水垢样品,向样品中逐滴加入稀盐酸,其变化关系如图所示,试计算:
热水瓶用久后,瓶胆内壁常附着一层水垢(主要成分是CaCO3和Mg(OH))2,其它成份忽略不计).某兴趣小组的同学为了探究水垢中Mg(OH)2的含量,取10g水垢样品,向样品中逐滴加入稀盐酸,其变化关系如图所示,试计算: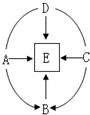 A~E是初中化学常见的物质,它们的相互关系如右图所示(图中“→”代表物质在一定条件下发生转化,“--”表示物质间可以相互反应).其中A和B都属于碳酸盐,且B可用于补钙,C是碱,E是最常用的溶剂.请回答下列问题:
A~E是初中化学常见的物质,它们的相互关系如右图所示(图中“→”代表物质在一定条件下发生转化,“--”表示物质间可以相互反应).其中A和B都属于碳酸盐,且B可用于补钙,C是碱,E是最常用的溶剂.请回答下列问题: