题目内容
2.某工厂排放的废液中含有少量硫酸和硫酸铜.小军同学取适量废液放入盛有一定量锌粉的烧杯中,搅拌,待充分反应后过滤,得少量滤渣和滤液.关于该实验,下列说法正确的是( )| A. | 发生的反应都是置换反应 | B. | 实验所得滤液是纯水,可直接排放 | ||
| C. | 滤渣中一定含铜和锌 | D. | 反应前后液体的酸性减弱,pH变小 |
分析 根据锌的金属活动性比铜、氢弱,能与硫酸铜、硫酸发生置换反应,取适量废液放入盛有一定量锌粉的烧杯中,锌先与硫酸铜溶液发生置换反应,生成硫酸锌溶液和铜,待硫酸铜溶液反应完,锌与硫酸反应生成硫酸锌和氢气,进行分析判断.
解答 解:A、锌与硫酸铜、硫酸的反应,均是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,均属于置换反应,故选项说法正确.
B、由于不知加入锌粉的质量,无法确定反应的程度,实验所得滤液不一定是纯水,若硫酸有剩余,实验所得滤液中含有硫酸,不能直接排放,故选项说法错误.
C、由于不知加入锌粉的质量,无法确定反应的程度,滤渣中一定含铜,不一定含锌,故选项说法错误.
D、反应前后液体的酸性减弱,pH变大,故选项说法错误.
故选:A.
点评 本题难度不是很大,熟练掌握金属的化学性质、综合考虑各种出现的情况是正确解答此类题的关键.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
13.变化无处不在,下列变化中属于物理变化的是( )
| A. | 燃放烟花 | B. | 风力发电 | C. | 金属冶炼 | D. | 粮食酿醋 |
10.“地沟油炼出生物柴油”,桐乡东江能源科技有限公司实现了变废为宝.生物柴油燃烧后SO2和颗粒物质排放很少,且CO等气体的排放量比化石燃料低11%--53%.由此可知使用生物燃油可以( )
| A. | 没有空气污染 | B. | 减少酸雨危害 | C. | 消除温室效应 | D. | 渡过能源危机 |
17.下列物质的变化,不能通过一步反应实现的是( )
| A. | Cu(OH)2→NaOH | B. | MgCl2→Mg(NO3)2 | C. | Cu(OH)2→CuSO4 | D. | CaCO3→CaO |
7.用CO2和NH3合成尿素[CO(NH2)2]是固定和利用CO2的成功范例,其反应的化学方程式为:CO2+2NH3═CO(NH2)2+H2O.下列说法正确的是( )
| A. | 尿素中有4个氢原子 | |
| B. | 氨气中氮元素的化合价为+3 | |
| C. | 如果有1个二氧化碳分子反应必然生成一个尿素分子 | |
| D. | 二氧化碳中的氧原子和水中的氧原子核内质子数不同 |
14.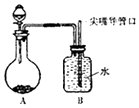 小明设计了趣味实验装置(如图所示),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )
小明设计了趣味实验装置(如图所示),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )
 小明设计了趣味实验装置(如图所示),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )
小明设计了趣味实验装置(如图所示),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )| A. | 氯化钠和水 | B. | 二氧化锰和过氧化氢溶液 | ||
| C. | 硝酸铵和水 | D. | 铜和稀硫酸 |
11.漂白粉的主要成分为次氯酸钙[Ca(ClO)2],作漂白剂用于造纸、纺织工业.Ca(ClO)2中氯元素的化合价为( )
| A. | +2 | B. | +3 | C. | +1 | D. | -1 |
12.从微观角度对宏观现象作出解释,是化学学习的重要观点.下列解释错误的是( )
| 选项 | 事实 | 解释 |
| A | 缉毒犬能根据气味发现毒品 | 分子在不断运动 |
| B | 用肉眼不能直接观察到二氧化碳分子 | 二氧化碳分子很小 |
| C | 冰受热变为水,水受热变为水蒸气 | 分子可以再分 |
| D | 固体碘受热升华 | 碘分子间的间隔增大 |
| A. | A | B. | B | C. | C | D. | D |
 梓檬酸(C6H8O7)是一种常见的有机酸,用棉花蘸取柠檬酸溶液,擦洗杯子内的茶渍.
梓檬酸(C6H8O7)是一种常见的有机酸,用棉花蘸取柠檬酸溶液,擦洗杯子内的茶渍.