题目内容
12.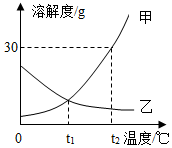 如图是甲、乙两种固体的溶解度曲线,下列说法中正确的是( )
如图是甲、乙两种固体的溶解度曲线,下列说法中正确的是( )| A. | t1℃时,甲和乙的溶质质量分数相等 | |
| B. | t2℃时,15g乙加到50g水中形成饱和溶液 | |
| C. | t2℃时,甲、乙饱和溶液降温至t1℃析出固体甲多余乙 | |
| D. | t2℃时,50g甲中加100g水得到33.3%的溶液 |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A、t1℃时,甲和乙物质的溶解度相等,所以饱和溶液的溶质质量分数相等,故A错误;
B、t2℃时,甲物质的溶解度是30g,所以15g乙加到50g水中形成饱和溶液,故B正确;
C、t2℃时,甲、乙饱和溶液的质量不能确定,所以降温至t1℃析出固体的质量也不能确定,故C错误;
D、t2℃时,甲物质的溶解度是30g,50g甲中加100g水得到溶液的质量分数为:$\frac{30g}{130g}$×100%=23.1%,故D错误.
故选:B.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
3.下列物质中属于纯净物的是( )
| A. | 空气 | B. | 液氧 | C. | 生铁 | D. | 粗盐 |
20.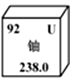 近期,由“朝核问题”引起的朝美对峙全球瞩目.铀浓缩技术是核问题的关键技术.如图是铀元素在元素周期表中的信息图,从中可以获得的信息是( )
近期,由“朝核问题”引起的朝美对峙全球瞩目.铀浓缩技术是核问题的关键技术.如图是铀元素在元素周期表中的信息图,从中可以获得的信息是( )
 近期,由“朝核问题”引起的朝美对峙全球瞩目.铀浓缩技术是核问题的关键技术.如图是铀元素在元素周期表中的信息图,从中可以获得的信息是( )
近期,由“朝核问题”引起的朝美对峙全球瞩目.铀浓缩技术是核问题的关键技术.如图是铀元素在元素周期表中的信息图,从中可以获得的信息是( )| A. | 该元素的相对原子质量为92 | B. | 该元素的原子序数为238 | ||
| C. | 一个铀原子的核外有92个质子 | D. | 该元素属于金属元素 |
7.下列实验操作正确的是( )
| A. |  滴加液体 | B. |  稀释浓硫酸 | C. | 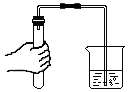 检查气密性 | D. | 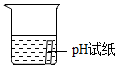 测定溶液pH |
17.下列物质敞口放置一段时间后,溶液变质且质量增大的是( )
| A. | 浓盐酸 | B. | 浓H2SO4 | C. | 烧碱溶液 | D. | 石灰水 |
3.25℃时,向饱和石灰水中加入少量生石灰并恢复到25℃.下列说法正确的是( )
| A. | 溶液中溶质的质量减少 | B. | 溶液中溶质的质量分数增大 | ||
| C. | 溶液的碱性增强 | D. | Ca(OH)2的溶解度增大 |
4.下列有关乙酸乙酯(化学式为C4H8O2)的叙述正确的是( )
| A. | 乙酸乙酯完全氧化后生成二氧化碳和水 | |
| B. | 乙酸乙酯由碳、氢、氧原子构成 | |
| C. | 乙酸乙酯中碳、氧元素的质量比为2:1 | |
| D. | 乙酸乙酯是由碳、氢、氧元素组成的氧化物 |