题目内容
14.某校化学兴趣小组在老师指导下探究孔雀石中的主要成份碱式碳酸铜的含量.他们取50克孔雀石粉末,在密闭容器中加热,观察到孔雀石分解过程中有水和能使澄清石灰水变浑浊的气体产生,绿色的孔雀石逐渐变为黑色粉末(氧化铜).经测定生成水3.6g,请分析数据,回答下列问题:(1)组成孔雀石的元素有4种;
(2)孔雀石中的碱式碳酸铜质量分数是多少(写出计算过程)?
分析 (1)从题目中我们可以看出所发生的反应是:碱式碳酸铜分解产生的二氧化碳、水和氧化铜,可以据此结合质量守恒定律进行解答;
(2)根据反应生成的水的质量结合反应的化学方程式可以计算出碱式碳酸铜的质量,进而求出其质量分数即可.
解答 解:(1)碱式碳酸铜分解产生的二氧化碳、水和氧化铜,根据反应前后元素的种类不变可以知道可以碱式碳酸铜是由Cu、C、O、H四种元素组成;
(2)设孔雀石中碱式碳酸铜的质量为x
Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O
222 18
x 3.6g
$\frac{222}{x}$=$\frac{18}{3.6g}$
解得:x=44.4g
孔雀石中的碱石碳酸铜质量分数是:$\frac{44.4g}{50g}$×100%=88.8%
答:孔雀石中的碱石碳酸铜质量分数是88.8%.
故答案为:(1)4;
(2)88.8%.
点评 本题主要考查了根据化学方程式的计算,解题的关键是会根据水的质量求算参加反应的碱式碳酸铜.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
2.我们每天生活在不断变化的物质世界里,以下变化属于化学变化的是( )
| A. | 冰雪融化 | B. | 干冰升华 | C. | 食物腐败 | D. | 菠萝榨汁 |
19.生活中处处离不开化学,下列说法错误的是( )
| A. | 胃酸过多的人要少喝碳酸饮料 | |
| B. | 蒸馏水绝对纯净,其中不含任何化学物质 | |
| C. | 动植物的新陈代谢过程属于缓慢氧化反应 | |
| D. | 空气中敞口放置的饼干变软是因为空气中含有水蒸气 |
6.世界卫生组织研究机构今年10月17日发布报告,首次指认大气污染“对人类致癌”,这向我们传递一个信号,必须采取有效措施,改善我们的环境.下列做法不利于保护环境的是( )
| A. | 倡导“节能减排、低碳出行”的生活方式,鼓励人们开汽车出行 | |
| B. | 增加城市绿地面积,合理使用化肥农药 | |
| C. | 实行垃圾分类回收再利用,杜绝露天焚烧秸秆 | |
| D. | 研制高性能的耐磨轮胎,可以减少细颗粒物(PM2.5)的产生 |

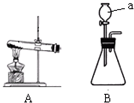 如图A、B为实验室制取气体的发生装置.
如图A、B为实验室制取气体的发生装置.