题目内容
17.在氢气与氧化钨的反应中:3H2+WO3$\stackrel{高温}{→}$W+3H2O,下列说法正确的是( )| A. | W是氧化剂 | B. | H2是还原剂 | ||
| C. | 氢元素的化合价没有改变 | D. | 该反应是分解反应 |
分析 根据氢气具有还原性,以及氧化还原反应的过程,元素化合价的变化以及反应类型来分析.
解答 解:A.W是生成物,是由三氧化钨失去氧形成的,属于还原产物,故错误;
B.氢气具有还原性,能将三氧化钨中的氧夺去形成单质钨,属于还原剂,故正确;
C.在反应物氢气中,氢元素为0价,在生成物水中氢元素显+1价,化合价发生了改变,故错误;
D.该反应是由一种单质与一种化合物反应生成另一种单质与另一种化合物,属于置换反应,故错误.
故选B.
点评 解答本题要充分理解氧化还原反应的含义,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
相关题目
7.高铁酸钾(K2FeO4)是一种集吸附、凝聚、杀菌等功能为一体的新型高效水处理剂,可将水中的三氯乙烯(C2HCl3)除去85.6%,下列说法正确的是( )
| A. | K2FeO4是氧化物 | B. | C2HCl3中三种元素质量比是2:1:3 | ||
| C. | K2FeO4中Fe元素的化合价为+3价 | D. | C2HCl3相对分子质量为131.5 |
8.2016年1月24日,全国迎来30年一遇寒潮,广东省大部分地区下起了雪花!在寒冷天气里,人们必须摄取足够的食物,以维持体温和健康.下列有关说法中正确的是( )
| A. | 人体缺钙易引起甲状腺肿大 | |
| B. | 蛋白质、糖类、油脂都属于有机物,在体内消化会放出热量,维持体温 | |
| C. | 缺锌会引起食欲不振,生长迟缓,发育不良,因此我们要大量补充葡萄糖酸锌 | |
| D. | 摄入过多的油脂容易引发肥胖和心脑血管疾病,因此我们不要吃油脂类食物 |
5.某化学兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数,取用2g石灰石样品,把20g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶解于水),每次充分反应后都经过滤、干燥、称量,得实验数据如表:
(1)从以上数据可知,这四次实验中,第4次石灰石样品中的碳酸钙已完全反应.
(2)石灰石样品中碳酸钙的质量分数为85%;
(3)计算该化学兴趣小组所用稀盐酸的溶质质量分数(需写出计算过程).
| 实验次数 | 1 | 2 | 3 | 4 |
| 稀盐酸的用量 | 5g | 5g | 5g | 5g |
| 剩余固体的质量 | 1.5g | 1.0g | 0.5g | 0.3g |
(2)石灰石样品中碳酸钙的质量分数为85%;
(3)计算该化学兴趣小组所用稀盐酸的溶质质量分数(需写出计算过程).
2.请回忆你和老师共同完成的酸和碱反应的实验探究,并按下列要求进行实验设计与分析:
【实验探究】
(1)请你依据图设计一个酸和碱反应的探究实验:
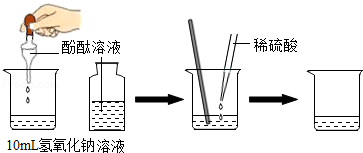
(2)为探究上述酸、碱反应后硫酸是否过量,甲、乙、丙三位同学设计了以下方案:
【实验评价】
①(2)中三个同学设计的三个方案中,有一个正确的方案,是丙(填“甲”、“乙”、“丙”)同学的方案.
②请分析另外两个同学方案错误的原因:一个同学方案错误的原因是生成硫酸钠,不管硫酸是否剩余,滴入氯化钡溶液都会生成沉淀,另一个同学方案错误的原因是硫酸过量酚酞也不变色(酚酞试液遇酸性或中性溶液都不变色).
③滴加硫酸时要用玻璃棒不断的搅拌,目的是使得物质充分混合,反应更加迅速.
【实验反思】
探究硫酸和氢氧化钠反应后硫酸是否有剩余,还可选择一种试剂镁.
【实验探究】
(1)请你依据图设计一个酸和碱反应的探究实验:

| 实验步骤 | 实验现象 | 结论 |
| ①向烧杯中加入10mL氢氧化钠溶液,并滴入几滴酚酞试液 | ①溶液颜色变红; | 酸和碱发生了中和反应 |
| ②再用滴管慢慢滴入稀硫酸,并不断搅拌溶液. | ②不断搅拌溶液至溶液颜色变成无色. |
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 甲同学的方案 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 硫酸过量 |
| 乙同学的方案 | 取样,滴入几滴无色酚酞溶液 | 酚酞溶液不变色 | 酸、碱恰好完全反应 |
| 丙同学的方案 | 取样,滴入几滴紫色石蕊溶液 | 溶液变红 | 硫酸过量 |
①(2)中三个同学设计的三个方案中,有一个正确的方案,是丙(填“甲”、“乙”、“丙”)同学的方案.
②请分析另外两个同学方案错误的原因:一个同学方案错误的原因是生成硫酸钠,不管硫酸是否剩余,滴入氯化钡溶液都会生成沉淀,另一个同学方案错误的原因是硫酸过量酚酞也不变色(酚酞试液遇酸性或中性溶液都不变色).
③滴加硫酸时要用玻璃棒不断的搅拌,目的是使得物质充分混合,反应更加迅速.
【实验反思】
探究硫酸和氢氧化钠反应后硫酸是否有剩余,还可选择一种试剂镁.
9.判断推理是学习化学常用的方思维方式,下列判断正确的是( )
| A. | 某固体物质加入稀盐酸能产生气体,则该固体可能是活泼金属 | |
| B. | 给水通直流电可以产生氢气和氧气,则水是由氢气和氧气组成的 | |
| C. | 同种元素的原子质子数相同,则质子数相同的微粒属于同种元素 | |
| D. | 中和反应的产物是盐和水,则生成盐和水的反应一定是中和反应 |
7.分析推理是化学学习中常用的思维方法.下列分析推理正确的是( )
| A. | 金刚石很硬,故石墨也很硬 | |
| B. | 空气中二氧化硫会造成酸雨,所以空气中二氧化碳一定会造成酸雨 | |
| C. | 离子是带电荷的微粒,所以带电荷的微粒一定是离子 | |
| D. | 同温下分解氯酸钾,加催化剂的反应速率快,故催化剂可以改变反应速率 |