题目内容
写出除去下列纯净物中少量杂质的试剂(括号内的物质为杂质).
(1)CO(CO2) ; (2)CO2(CO) ;
(3)Cu(Fe) ; (4)FeCl2溶液(CuCl2溶液) .
(1)CO(CO2)
(3)Cu(Fe)
考点:物质除杂或净化的探究,常见气体的检验与除杂方法,金属的化学性质,盐的化学性质
专题:物质的分离、除杂、提纯与共存问题
分析:根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答:解:(1)CO2能与氢氧化钠溶液反应生成碳酸钠和水,CO不与氢氧化钠溶液反应,能除去杂质且没有引入新的杂质,符合除杂原则.
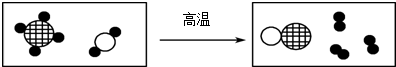
(2)CO能与灼热的氧化铜反应生成铜和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则.
(3)根据金属活动性顺序,铁能和酸反应,铜和酸不反应,故可用盐酸(或稀硫酸)除去铁,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则.
(4)要除去FeCl2溶液中的CuCl2,实质就是除去铜离子,可利用CuCl2溶液与铁粉反应生成氯化亚铁溶液和铜,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则.
故答案为:(1)氢氧化钠溶液;(2)灼热的氧化铜;(3)盐酸(或稀硫酸)等;(4)铁粉.
(2)CO能与灼热的氧化铜反应生成铜和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则.
(3)根据金属活动性顺序,铁能和酸反应,铜和酸不反应,故可用盐酸(或稀硫酸)除去铁,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则.
(4)要除去FeCl2溶液中的CuCl2,实质就是除去铜离子,可利用CuCl2溶液与铁粉反应生成氯化亚铁溶液和铜,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则.
故答案为:(1)氢氧化钠溶液;(2)灼热的氧化铜;(3)盐酸(或稀硫酸)等;(4)铁粉.
点评:物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
相关题目
下列符号中,既能表示一种元素,又能表示该元素的一个原子,还能表示该元素所形成的单质的是( )
| A、K | B、N |
| C、H2 | D、CO |
已知三种二价金属的活动性顺序为X>Y>Z,某同学设计进行了如下实验,请你从理论上分析肯定不成功的实验是( )
| A、实验一:X+YSO4→XSO4+Y |
| B、实验二:Z+YSO4→ZSO4+Y |
| C、实验三:X+H2SO4→XSO4+H2↑ |
| D、实验四:Z+H2SO4(稀)→不反应 |
下列变化中属于物理变化的是( )
| A、燃放烟花 | B、食物腐烂 |
| C、剪贴窗花 | D、钢铁生锈 |
下列化学方程式书写错误的是( )
| A、HCl+NaOH=NaCl+H2O | ||||
B、C2H5OH+3O2
| ||||
| C、Zn+2HCl=ZnCl2+H2↑ | ||||
| D、Fe2O3+2H2SO4═2FeSO4+2H2O |