题目内容
12.下列字母A~E表示初中化学的常见物质,它们由氢、碳、氧、氯、钠、钙、铁中的2~3种元素组成.已知:①CaCl2、NaCl溶液遇酚酞不变色,Na2CO3溶液遇酚酞显红色;
②Na2CO3+CaCl2═CaCO3↓+2NaCl.
(1)A由3种元素组成,常用于建筑材料和改良酸性土壤,A的俗称是熟石灰(或消石灰).
(2)B是一种氧化物.向 D的溶液中加入固体B,固体溶解同时溶液由无色变成黄色,B的化学式为Fe2O3.
(3)向D的溶液中加E的溶液,产生无色气体,反应的化学方程式为2HCl+Na2CO3=2NaCl+CO2↑+H2O.
(4)向D的溶液中加A的溶液,无明显现象,再向混合溶液中滴加酚酞,溶液仍为无色,则所得溶液中的溶质可能为CaCl2;CaCl2和HCl(写出所有可能).
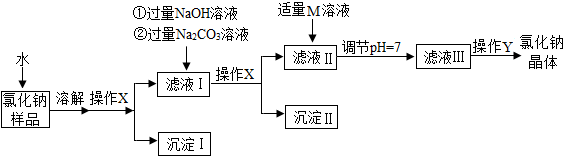
(5)将(3)和(4)所得溶液混合,得到溶液X,依据混合过程中观察到的冒气泡及产生白色沉淀、溶液变红的现象,可以确定溶液X中的溶质.
分析 (1)根据“A由3种元素组成,常用于建筑材料和改良酸性土壤”,推测A为氢氧化钙;
(2)根据“B是一种氧化物”,“向D的溶液中加入固体B,固体溶解同时溶液由无色变成黄色”,推测B的为氧化铁.
(3)根据“向D的溶液中加E的溶液,产生无色气体”,考虑碳酸钠与稀盐酸反应.
(4)根据“向D的溶液中加A的溶液,无明显现象,再向混合溶液中滴加酚酞,溶液仍为无色”说明溶液为中性,则氢氧化钙与稀盐酸恰好反应,或酸过量;
(5)将(3)和(4)所得溶液混合,得到溶液X,依据混合过程中观察到的冒气泡及产生白色沉淀、溶液变红的现象,推测氢氧化钙、碳酸钠、稀盐酸是否反应.
解答 解:
下列字母A~E表示初中化学的常见物质,它们由氢、碳、氧、氯、钠、钙、铁中的2~3种元素组成.
已知:①CaCl2、NaCl溶液遇酚酞不变色,Na2CO3溶液遇酚酞显红色;
②Na2CO3+CaCl2═CaCO3↓+2NaCl.
(1)根据“A由3种元素组成,常用于建筑材料和改良酸性土壤”,推测A为氢氧化钙,其俗称是熟石灰(或消石灰).
(2)根据“B是一种氧化物”,“向D的溶液中加入固体B,固体溶解同时溶液由无色变成黄色”,推测B的为氧化铁,氧化铁与物质D为稀盐酸反应得黄色溶液,故B的化学式为Fe2O3.
(3)根据“向D的溶液中加E的溶液,产生无色气体”,考虑碳酸钠与D物质稀盐酸反应,故其反应的化学方程式为2HCl+Na2CO3=2NaCl+CO2↑+H2O.
(4)根据“向D的溶液中加A的溶液,无明显现象,再向混合溶液中滴加酚酞,溶液仍为无色”说明溶液为中性,则氢氧化钙与稀盐酸恰好反应,或酸过量,故所得溶液中的溶质可能为CaCl2;CaCl2和HCl.
(5)将(3)和(4)所得溶液混合,得到溶液X,依据混合过程中观察到的冒气泡及 产生白色沉淀、溶液变红的现象,可以确定溶液X中的溶质.
故答案为:
(1)熟石灰(或消石灰);(2)Fe2O3;(3)2HCl+Na2CO3=2NaCl+CO2↑+H2O;
(4)CaCl2;CaCl2和HCl;(5)产生白色沉淀、溶液变红
点评 本题的推断由组成物质的元素做为限定条件,因此,熟悉常见物质的组成、性质及变化规律对该题中所涉及物质的推断就至关重要了.

 应用题作业本系列答案
应用题作业本系列答案同学们通过实验制取精盐进行了思考.
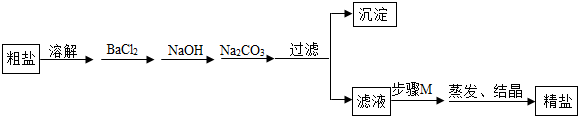
实验过程:
查阅资料:
①一般除杂过程中所加入的试剂均稍过量.
②部分酸、碱和盐的溶解性表(室温):
| / | OH- | Cl- | SO42- | CO32- |
| H+ | 溶、挥 | 溶 | 溶、挥 | |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 不 | 不 |
| Mg2+ | 不 | 溶 | 溶 | 微 |
反思评价:
(1)加入BaCl2的化学方程式是BaCl2+MgSO4=BaSO4↓+MgCl2;加入NaOH的目的是除去氯化镁,化学方程式是MgCl2+2NaOH═Mg(OH)2↓+2NaCl.
(2)有同学认为没有必要加入Na2CO3,你的观点是有必要加入碳酸钠,除去过量的氯化钡.
(3)步骤M中所加物质是稀盐酸.
| A. |  向一定量稀硫酸中加入NaOH溶液 | |
| B. |  向一定量稀盐酸中加入铁粉 | |
| C. |  向一定量CaCl2、CaCO3固体混合物中加入稀盐 | |
| D. | 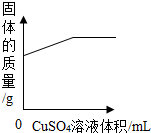 向一定量铁粉中加入CuSO4溶液 |
| A. | 用灯帽盖灭酒精灯--隔绝空气 | |
| B. | 森林灭火时,建立隔离带--隔绝可燃物 | |
| C. | 家具起火,用水扑灭--降低温度 | |
| D. | 煤炉生火时,用木柴引燃--提高着火点 |
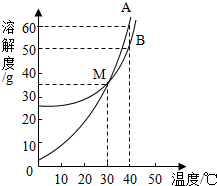 A、B两种物质的溶解度曲线如图.
A、B两种物质的溶解度曲线如图.