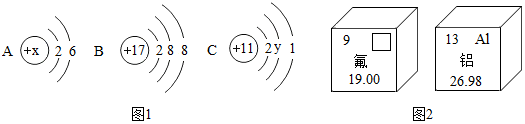
题目内容
11.将甲、乙、丙、丁四种物质加入到一密闭容器内,在一条条件下发生化学反应,反应前后各物质的质量变化如图所示: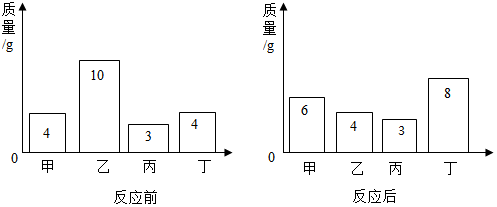
根据四种物质的前后质量的变化,可知该容器内发生化学反应的类型为( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
分析 根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.反应后质量增加的是生成物,减少的是反应物,据此分析
解答 解:根据质量守恒定律,反应后质量多了,是生成物,反应后质量少了是反应物,反应后质量不变,可能是催化剂,可能没参加反应,故乙为反应物,甲、丁为生成物,丙可能为催化剂,该反应为分解反应.
故选B.
点评 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.

暑假,同学们在帮忙老师整理实验室时,发现一瓶石灰水试剂瓶瓶壁和瓶塞周围有一些白色粉末.为了弄清楚白色粉末的成分及形成原因,他们进行了如下探究:
(1)对白色粉末成分的猜想和成因分析:
白色粉末的成分 | 形成的原因 |
可能是CaCO3 | 石灰水与空气中CO2反应; 化学方程式为:__ |
可能是_______ | 暑假气温较高,溶质的溶解度降低或溶剂蒸发,石灰水中的溶质结晶析出 |
经过反复思考,同学们认为白色粉末还可能是__的混合物.
(2)设计实验:甲同学取白色粉末装入试管中,加入少量的水、振荡,发现有白色固体不溶解,于是他得出粉末中一定有CaCO3的结论.乙同学查阅了溶解性表(如下图),认为甲同学的结论不严密,理由是:__.
OH﹣ | Cl﹣ | CO32﹣ | NO3﹣ | |
Ca2+ | 微 | 溶 | 不 | 溶 |
为了得出较严密的结论,他们进行了如下实验,请完成下列实验报告:
实验步骤 | 可能观察到的现象 | 结论 |
取上述试管中的上层清夜,滴加1~2无色酚酞试液 | __ | __ |
往上述试管中的残留的固体中加入稀硫酸 | __ | 白色粉末中__(“有”或“无”)CaCO3 |
由上述实验可知白色粉末的成分是:__ | ||
(3)交流与反思
①通过上述实验的探究,同学们向实验室提出保存、使用易变质的溶液时的下列建议,合理的是__.
A.密封保存B.使用前,临时配制C.禁止使用这种试剂
②实验室清洗装石灰水试剂瓶内壁上的白色粉末时,可用稀盐酸,请写出其中可能发生的反应的化学方程式(写出一个即可):__.
 20℃时,在两只烧杯中加入相同质量的水,再分别加入相同质量的氯化钠和蔗糖固体,充分溶解后,结果如图所示,下列说法正确的是( )
20℃时,在两只烧杯中加入相同质量的水,再分别加入相同质量的氯化钠和蔗糖固体,充分溶解后,结果如图所示,下列说法正确的是( )| A. | 两烧杯中的溶液质量相等 | B. | 20℃时两者的溶解度相等 | ||
| C. | 氯化钠溶液一定是饱和溶液 | D. | 蔗糖溶液一定是饱和溶液 |
| A. | Mg>Ag>X | B. | Mg>X>Ag | C. | Ag>X>Mg | D. | X>Mg>Ag |