题目内容
5.制作松花蛋所用的配料主要有纯碱、食盐、生石灰、草木灰、水等.食用新制的松花蛋时常有涩味,可在食用前加调味品去掉,这种调味品最好是( )
| A. | 食盐 | B. | 食醋 | C. | 酱油 | D. | 香油 |
分析 由题意可知,制作松花蛋所用的配料主要有纯碱、食盐、生石灰、草木灰、水等;生石灰是氧化钙的俗称,能与反应生成氢氧化钙;纯碱是碳酸钠的俗称,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,生成的氢氧化钠具有涩味,据此进行分析判断.
解答 解:制作松花蛋所用的配料主要有纯碱、食盐、生石灰、草木灰、水等;生石灰是氧化钙的俗称,能与反应生成氢氧化钙;纯碱是碳酸钠的俗称,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,生成的氢氧化钠具有涩味.
为了减轻涩味,可在食用时添加酸性调味品.食醋显酸性,符合要求.
故选:B.
点评 本题难度不大,掌握盐的化学性质、生石灰的化学性质、酸的化学性质并能灵活运用是正确解答本题的关键.

练习册系列答案
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
13.小强同学看到妈妈将买来的排水口洗净剂(主要成分:过碳酸钠、柠檬酸)洒在厨房排水口网状盖的底部,倒上温水后迅速冒出气泡.为了解其反应过程,他与学习小组的同学进行了如下探究.
(1)实验过程:教师提供了一瓶过碳酸钠(Na2CO4),小组同学进行了如下实验探究:
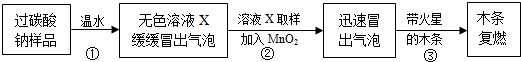
(2)提出问题:无色溶液X中的溶质有哪些物质?
(3)猜想与假设:根据以上实验现象,X溶液中一定存在的溶质是H2O2;还可能存在Na2CO3、NaHCO3、NaOH中的一种或几种.
(4)查找资料:
资料1:氯化钙溶液呈中性;氯化钙溶液与碳酸氢钠溶液混合不发生反应;
氯化钙溶液与碳酸钠溶液混合后发生如下反应:Na2CO3+CaCl2═CaCO3↓+2NaCl.
资料2:NaHCO3溶液呈碱性,与石灰水反应生成白色沉淀;碳酸氢钠、碳酸钠与足量的酸反应产物相同.
(5)实验过程:小组同学对溶液X中的溶质进行了如下实验.请将下列实验方案填写完整.
(6)实验反思:根据资料,NaHCO3溶液能与石灰水反应生成白色沉淀.于是,同学们猜想:碳酸氢钠与氢氧化钠是否可以发生NaHCO3+NaOH=Na2CO3+H2O(写方程式)这样的反应?于是,同学们进行了新的探究实验.
(1)实验过程:教师提供了一瓶过碳酸钠(Na2CO4),小组同学进行了如下实验探究:
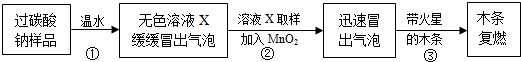
(2)提出问题:无色溶液X中的溶质有哪些物质?
(3)猜想与假设:根据以上实验现象,X溶液中一定存在的溶质是H2O2;还可能存在Na2CO3、NaHCO3、NaOH中的一种或几种.
(4)查找资料:
资料1:氯化钙溶液呈中性;氯化钙溶液与碳酸氢钠溶液混合不发生反应;
氯化钙溶液与碳酸钠溶液混合后发生如下反应:Na2CO3+CaCl2═CaCO3↓+2NaCl.
资料2:NaHCO3溶液呈碱性,与石灰水反应生成白色沉淀;碳酸氢钠、碳酸钠与足量的酸反应产物相同.
(5)实验过程:小组同学对溶液X中的溶质进行了如下实验.请将下列实验方案填写完整.
| 实验操作 | 主要实验现象 | 结论 |
| ① | 证明溶液中有Na2CO3 | |
| ② | 证明溶液中无NaHCO3 | |
| ③ | 证明溶液中无NaOH |
14.“民以食为天,食以安为先”.下列做法不会危及人体健康的是( )
| A. | 用工业盐作调味品 | B. | 用霉变花生压榨食用油 | ||
| C. | 常食用烧烤类食品 | D. | 用干冰保存食品 |

 化学电池是一类重要的能源,按工作性质可分为:一次电池(例如干电池)和二次电池(可充电电池,例如铅酸蓄电池).请简要回答下列各空
化学电池是一类重要的能源,按工作性质可分为:一次电池(例如干电池)和二次电池(可充电电池,例如铅酸蓄电池).请简要回答下列各空