题目内容
11.某班同学为验证酸的化学通性,做了五组实验.分析并回答问题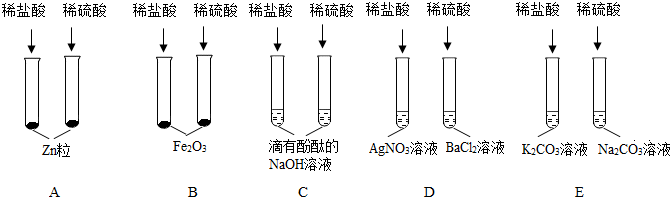
(1)A组试管中都产生H2.若要制得较纯的H2,选稀硫酸而不是盐酸的原因是盐酸具有挥发性,挥发出氯化氢气体,使制得的氢气中混有氯化氢气体.
(2)B组试管中实验现象相同,该现象是红棕色固体逐渐减少,溶液变成黄色.
(3)写出C组任一试管中发生反应的化学方程式NaOH+HCl=NaCl+H2O.
(4)上述五组实验中只有A 组发生反应的基本类型与其它四组的基本反应类型不同.
分析 (1)根据盐酸具有挥发性,进行分析解答.
(2)根据氧化铁能与酸反应生成盐和水,进行分析解答.
(3)氢氧化钠溶液能与盐酸、硫酸发生中和反应生成盐和水,据此进行分析解答.
(4)根据反应的基本类型进行分析解答.
解答 解:(1)盐酸具有挥发性,挥发出氯化氢气体,制得的氢气中混有氯化氢气体,不纯净.
(2)氧化铁能与稀盐酸、稀硫酸反应生成氯化铁和水、硫酸铁和水,生成的氯化铁、硫酸铁溶液显黄色,会观察到红棕色固体逐渐减少,溶液变成黄色.
(3)氢氧化钠与硫酸反应生成硫酸钠和水,与盐酸反应生成氯化钠和水,反应的化学方程式分别为2NaOH+H2SO4=Na2SO4+2H2O、NaOH+HCl=NaCl+H2O.
(4)酸能与酸碱指示剂、活泼金属、金属氧化物、碱、盐等反应,BCE分别复分解反应,A为置换反应,故选A.
故答案为:(1)盐酸具有挥发性,挥发出氯化氢气体,使制得的氢气中混有氯化氢气体;
(2)红棕色固体逐渐减少,溶液变成黄色;
(3)NaOH+HCl=NaCl+H2O或2NaOH+H2SO4=Na2SO4+2H2O;
(4)A.
点评 本题难度不大,掌握酸的化学性质(能与活泼金属、金属氧化物、碱、碳酸盐等反应)、物理性质并能灵活运用是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.下列实验操作不正确的是( )
| A. | 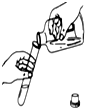 | B. |  | C. |  | D. | 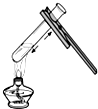 |
2.下列过程中,只发生物理变化的是( )
| A. | 风力发电 | B. | 葡萄酿酒 | C. | 钢铁生锈 | D. | 燃放焰火 |
19.下列叙述不正确的是( )
| A. | pH=7的溶液是中性溶液 | B. | 用食醋除去水壶中的水垢 | ||
| C. | 用稀盐酸除去铁制品上的锈 | D. | 酸雨就是指呈酸性的雨水 |
6.能闻到花香的原因是( )
| A. | 分子的质量和体积都很小 | B. | 分子间有间隔 | ||
| C. | 分子在不断运动 | D. | 分子由原子构成 |
16.下列实验合理的是( )
| A. | 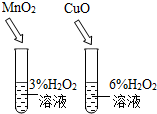 比较催化效果 | B. | 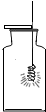 铁丝在纯氧中燃烧 | ||
| C. | 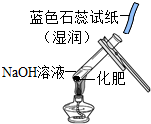 检验铵态氮肥 | D. | 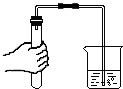 检查装置气密性 |
3.今年春季以来,我国许多城市雾霾天气频发,PM2.5是造成雾霾天气的“元凶”之一.PM2.5是用来监测空气中下列哪项含量的( )
| A. | 可吸入颗粒物 | B. | 二氧化氮 | C. | 二氧化碳 | D. | 一氧化碳 |