题目内容
32.5g锌可以跟200g硫酸溶液恰好完全反应.计算:
(1)可制得氢气多少克?
(2)这种硫酸溶液中溶质的质量分数是多少?
(1)可制得氢气多少克?
(2)这种硫酸溶液中溶质的质量分数是多少?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)根据题中的反应原理写出硫酸和锌反应的方程式,然后根据题中的比例关系和所给的数据列出比例关系解出需要的量;
(2)根据反应计算出32.5g恰好完全反应消耗硫酸的质量,利用溶质质量分数公式计算稀硫酸溶液的质量分数
(2)根据反应计算出32.5g恰好完全反应消耗硫酸的质量,利用溶质质量分数公式计算稀硫酸溶液的质量分数
解答:解:设反应放出氢气质量为x,消耗硫酸质量为y
Zn+H2SO4 ═ZnSO4 +H2↑
65 98 2
32.5g y x
=
=
x=1g
y=49g
(2)硫酸溶液中溶质的质量分数为:
×100%=24.5%
答:(1)可制得氢气为1g
(2)这种硫酸溶液中溶质质量分数是24.5%.
Zn+H2SO4 ═ZnSO4 +H2↑
65 98 2
32.5g y x
| 65 |
| 2 |
| 32.5g |
| x |
| 65 |
| 98 |
| 32.5g |
| y |
x=1g
y=49g
(2)硫酸溶液中溶质的质量分数为:
| 49g |
| 200g |
答:(1)可制得氢气为1g
(2)这种硫酸溶液中溶质质量分数是24.5%.
点评:本题主要考查学生运用化学方程式和溶质质量分数公式进行计算的能力.

练习册系列答案
相关题目
下列事实可用金属活动性强弱顺序加以解释的是( )
| A、铁的导热性能比铝的好 |
| B、不能用铁制容器配制硫酸铜溶液 |
| C、自然界中,铝元素含量比铁元素的高 |
| D、日常生活中,铝制品比铁制品更耐用 |
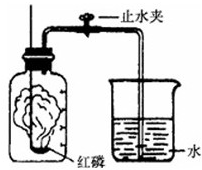 某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下: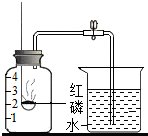 如图是初中化学教材中的一个装置示意图,请据图回答问题:
如图是初中化学教材中的一个装置示意图,请据图回答问题: