题目内容
20.下列化学方程式符合题意且书写正确的是( )| A. | 向稀硫酸溶液中通直流电:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2+O2↑ | |
| B. | 冬天用煤炉烤火造成煤气中毒:2C+O2═2CO | |
| C. | 用二氧化碳生产碳酸饮料:CO2+H2O═H2CO3 | |
| D. | 证明铝是金属活动性顺序表中氢之前的金属:Al+2HCl═AlCl2+H2↑ |
分析 A、向稀硫酸溶液中通直流电时,水分解生成氢气和氧气;
B、碳不完全燃烧生成一氧化碳;
C、二氧化碳和水反应生成碳酸;
D、铝和稀盐酸反应生成氯化铝和氢气.
解答 解:A、电解水的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,该选项书写不正确;
B、碳不完全燃烧的化学方程式为:2C+O2$\frac{\underline{\;不完全燃烧\;}}{\;}$2CO,该选项书写不正确;
C、二氧化碳和水反应的化学方程式为:CO2+H2O═H2CO3,该选项书写正确;
D、铝和稀盐酸反应的化学方程式为:2Al+6HCl═2AlCl3+3H2↑,该选项书写不正确.
故选:C.
点评 书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
8.关于“物质的燃烧的主要现象--所属反应类型”的描述正确的是( )
| A. | 碳在空气中燃烧发出白光--化合反应 | |
| B. | 硫在氧气中燃烧产生淡蓝色火焰--氧化反应 | |
| C. | 铁在氧气中剧烈燃烧,火星四射--化合反应 | |
| D. | 红磷在空气中燃烧产生大量白雾--化合反应 |
12.实验室可利用碱式碳酸铜(化学式:Cu2(OH)2CO3)制备氧化铜,并进行碳粉还原氧化铜的实验.
①制备氧化铜并检验产物,装置如图1所示(省略夹持仪器):已知烧碱可与二氧化碳反应,无水硫酸铜为白色固体可吸收水、变蓝.
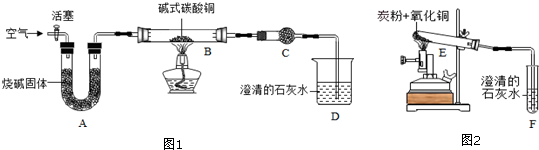
步骤一:连接A和B,打开活塞,通入空气.
步骤二:关闭活塞,连上C和D,开始加热.
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热.
B中发生反应的化学方程式为:□Cu2(OH)2CO3═□CuO+□H2O+□CO2↑
请在□中填入配平后的系数,依次为1、2、1、1.C中试剂是无水硫酸铜 无水硫酸铜.A的作用是吸收空气中的水蒸气和二氧化碳 水蒸气和二氧化碳,防止对产物检验造成干扰.选择t3时停止加热的理由是固体质量不再减少,证明碱式碳酸铜已经完全分解
②一定量碳粉还原①中制得的氧化铜并检验产物,装置如图2所示:实验过程中,观察到F中溶液变浑浊,E中的现象是黑色粉末变成红色,反应完全后,若仅撤走酒精喷灯停止加热,可能导致的后果是F中的液体通过导管流入E中,造成试管炸裂
③分析:若①中省略步骤三,对②中反应产物判断可能产生的影响及其原因.不能确定炭粉还原氧化铜的生成物中是否含有二氧化碳.
因为可能有①中未分解的碱式碳酸铜在实验②中分解,产生二氧化碳气体,干扰对炭粉还原氧化铜反应生成物的判断.
①制备氧化铜并检验产物,装置如图1所示(省略夹持仪器):已知烧碱可与二氧化碳反应,无水硫酸铜为白色固体可吸收水、变蓝.

步骤一:连接A和B,打开活塞,通入空气.
步骤二:关闭活塞,连上C和D,开始加热.
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热.
| 加热时间(min) | 0 | t1 | t2 | t3 |
| B中固体质量(g) | 6.66 | 5.20 | 4.80 | 4.80 |
请在□中填入配平后的系数,依次为1、2、1、1.C中试剂是无水硫酸铜 无水硫酸铜.A的作用是吸收空气中的水蒸气和二氧化碳 水蒸气和二氧化碳,防止对产物检验造成干扰.选择t3时停止加热的理由是固体质量不再减少,证明碱式碳酸铜已经完全分解
②一定量碳粉还原①中制得的氧化铜并检验产物,装置如图2所示:实验过程中,观察到F中溶液变浑浊,E中的现象是黑色粉末变成红色,反应完全后,若仅撤走酒精喷灯停止加热,可能导致的后果是F中的液体通过导管流入E中,造成试管炸裂
③分析:若①中省略步骤三,对②中反应产物判断可能产生的影响及其原因.不能确定炭粉还原氧化铜的生成物中是否含有二氧化碳.
因为可能有①中未分解的碱式碳酸铜在实验②中分解,产生二氧化碳气体,干扰对炭粉还原氧化铜反应生成物的判断.
 张飞家使用了天然气为燃料的管道燃气.为防止燃气泄露造成危险,家中安装了如图所示报警器.请回答:
张飞家使用了天然气为燃料的管道燃气.为防止燃气泄露造成危险,家中安装了如图所示报警器.请回答: