题目内容
溶液的微粒构成决定其性质,溶液的宏观组成是其成分计算的依据.
(1)氯化钠晶体是由 、Cl﹣ (填微粒符号)构成的.氯化钠溶于水,溶液导电能力显著增强,是因为其溶液中含有 ;而蔗糖溶于水,溶液很难导电,是因为 的缘故.
(2)用溶质质量分数为15%的氯化钠溶液来配制500g溶质质量分数为6%的氯化钠溶液,需要15%的氯化钠溶液 g.
(3)某温度下饱和氯化钠溶液的溶质质量分数为26%,试列式计算该温度下氯化钠的溶解度S(计算结果保留小数点后一位).
解:(1)氯化钠晶体是由Na+、Cl﹣构成的.氯化钠溶于水,溶液导电能力显著增强,是因为其溶液中含有较多的自由移动的离子;而蔗糖溶于水,溶液很难导电,是因为蔗糖在水中以分子形式存在,溶液中不存在自由移动带电的离子;
(2)需要15%的氯化钠溶液质量: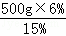 =200g;
=200g;
(3)由题意可得, =26%;
=26%;
解得:S=35.1g
答案:(1)Na+、Cl﹣;较多的自由移动的离子;蔗糖在水中以分子形式存在,溶液中不存在自由移动带电的离子;
(2)200;
(3)35.1g.

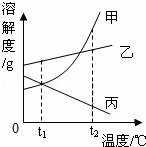
如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线.现有t2℃时甲、乙、丙三种物质的饱和溶液(无固体存在).下列说法正确的是( )
|
| A | 将原饱和溶液温度由t2℃降到t1℃时,所得三种溶液一定都是饱和溶液 |
|
| B | 将原饱和溶液分别蒸发等量水后恢复至t2℃时,析出溶质的质量丙>乙>甲 |
|
| C | 将原饱和溶液温度由t2℃降到t1℃时,所得溶液中溶质的质量分数由大到小的顺序为:乙>甲>丙 |
|
| D | 将原饱和溶液温度由t2℃降到t1℃时,析出甲的质量一定比乙多 |
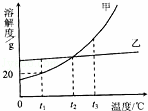
甲、乙两种固体物质(不含结晶水)的溶解度曲线如图,下列说法中正确的是( )
 2
2
|
| A. | t1℃甲的溶解度大于乙的溶解度 |
|
| B. | 溶解度受温度影响乙比甲大 |
|
| C. | t2℃甲乙两种物质饱和溶液中溶质质量分数相等 |
|
| D. | t3℃甲乙两种物质的饱和溶液降温至t1℃,析出溶质多的是甲 |
小瑾同学用图表对所学知识进行归纳,其中甲包含乙和丙,不包含丁,下列关系错误的是( )
| 甲 | 乙 | 丙 | 丁 | |
| A | 碱 | 烧碱 | 氢氧化钾 | 纯碱 |
| B | 合成材料 | 塑料 | 合成纤维 | 合成橡胶 |
| C | 溶液 | 糖水 | 生理盐水 | 泥浆 |
| D | 化石燃料 | 石油 | 煤 | 酒精 |

|
| A. | A | B. | B | C. | C | D. | D |
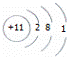 A.该粒子原子核内有11个质子
A.该粒子原子核内有11个质子