题目内容
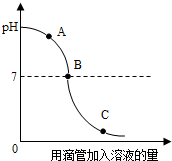 (2012?烟台)实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示曲线.下列有关该实验事实的说法正确的是( )
(2012?烟台)实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示曲线.下列有关该实验事实的说法正确的是( )分析:氢氧化钠溶液呈碱性,其pH大于7,盐酸呈酸性,其pH小于7,氢氧化钠溶液和盐酸可以发生中和反应,恰好完全反应时其pH等于7,氢氧化钠过量时显碱性,盐酸过量时显酸性.
解答:解:A、根据图象可以看出,开始时溶液的pH大于7,溶液呈碱性,故是向氢氧化钠溶液中加入稀盐酸,故A错误;
B、B点对应的pH等于7,表明氢氧化钠溶液和稀盐酸恰好完全反应,故B正确;
C、从图象可以看出,A点溶液呈碱性,酚酞试液在碱性溶液中显红色,故C说法正确;
D、C点的pH继续减小,说明酸还没有完全反应,故溶液中含有氯化氢溶质,故D错误,
故选BC.
B、B点对应的pH等于7,表明氢氧化钠溶液和稀盐酸恰好完全反应,故B正确;
C、从图象可以看出,A点溶液呈碱性,酚酞试液在碱性溶液中显红色,故C说法正确;
D、C点的pH继续减小,说明酸还没有完全反应,故溶液中含有氯化氢溶质,故D错误,
故选BC.
点评:本题以图象的形式考查了酸碱中和反应过程中溶液pH的变化,完成此题,要抓住曲线变化的趋势和关键点的意义.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
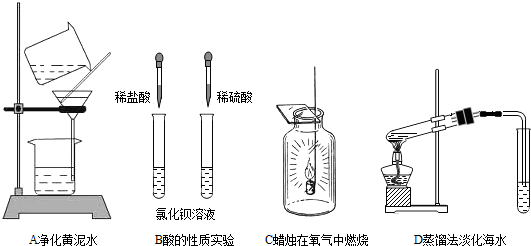
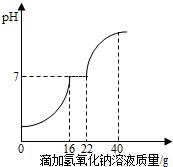 (2012?烟台)在学习酸的性质时,同学们发现实验室的工业盐酸呈黄色,老师解释说是应为里面含有氯化铁.为测定这瓶工业盐酸中氯化铁的含量(假设不含其他杂质),小霞做了如下实验:取20g工业盐酸加入到小烧杯中,然后向小烧杯中不断滴加溶质质量分数为10%的氢氧化钠溶液,同时用电子pH计不断读取反应时的pH,得出如右图所示的关系.求该工业盐酸中氯化铁的溶质质量分数.(结果保留至0.1%)
(2012?烟台)在学习酸的性质时,同学们发现实验室的工业盐酸呈黄色,老师解释说是应为里面含有氯化铁.为测定这瓶工业盐酸中氯化铁的含量(假设不含其他杂质),小霞做了如下实验:取20g工业盐酸加入到小烧杯中,然后向小烧杯中不断滴加溶质质量分数为10%的氢氧化钠溶液,同时用电子pH计不断读取反应时的pH,得出如右图所示的关系.求该工业盐酸中氯化铁的溶质质量分数.(结果保留至0.1%)