题目内容
19.欲测定大理石样品中CaCO3的质量分数.某同学设计了下图的装置.(提示:杂质不与稀盐酸反应;浓硫酸具有吸水性).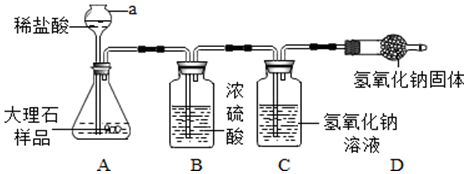
(1)仪器a的名称是长颈漏斗,装置A中反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O.
(2)在实验中装置C的作用是吸收产生的二氧化碳气体;要测定大理石样品中CaCO3的质量分数,除了加入足量的稀盐酸,还需要测量的数据是①③.(填选项);
①大理石样品的质量 ②浓硫酸实验前后的质量
③氢氧化钠溶液实验前后的质量 ④稀盐酸的质量分数
(3)实验结果测得CaCO3的质量分数往往偏小,原因是A、B装置中残存的CO2不能被C装置中的氢氧化钠充分吸收.
分析 (1)根据仪器用途写出名称,根据书写方程式原则写方程式;
(2)根据氢氧化钠的作用分析,根据纯度的计算公式$\frac{碳酸钙质量}{大理石质量}$×100%分析;
(3)根据纯度计算公式分析质量分数偏小的原因.
解答 解:(1)根据仪器用途写出名称,a为长颈漏斗,可以添加液体,大理石和稀盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O.
(2)装置C氢氧化钠溶液是吸收二氧化碳的,要测定大理石中碳酸钙的质量分数,加入足量盐酸后,可通过测定氢氧化钠溶液增重的质量求出二氧化碳的质量,根据二氧化碳的质量求出碳酸钙的质量,从而求出其质量分数.故选①③.
(3)测得碳酸钙的质量分数偏小是因为生成的二氧化碳没有全部转移到C装置中,使二氧化碳质量偏小,从而求出的碳酸钙质量偏小.
故答案为:(1)长颈漏斗,添加液体,CaCO3+2HCl=CaCl2+CO2↑+H2O;
(2)吸收产生的二氧化碳气体; ①③;
(3)A、B装置中残存的CO2不能被C装置中的氢氧化钠充分吸收.
点评 本题考查物质纯度的计算以及实验过程中造成误差原因的分析,是实验与计算相结合的题目,培养学生的思维综合能力

练习册系列答案
相关题目
9.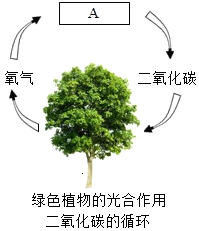 二氧化碳占空气总体积的0.03%,自然界中二氧化碳的循环如图所示,在A处不参与该循环的是( )
二氧化碳占空气总体积的0.03%,自然界中二氧化碳的循环如图所示,在A处不参与该循环的是( )
 二氧化碳占空气总体积的0.03%,自然界中二氧化碳的循环如图所示,在A处不参与该循环的是( )
二氧化碳占空气总体积的0.03%,自然界中二氧化碳的循环如图所示,在A处不参与该循环的是( )| A. | 人和动物的呼吸 | B. | 含碳燃料的燃烧 | C. | 发展利用太阳能 | D. | 植物的呼吸作用 |
14.在化学世界里没有生命的阿拉伯数字也变得鲜活起来,它们在不同的位置表示着不同的含义.下列化学符号中数字“2”表示的意义正确的是( )
| A. | CO2:一个二氧化碳分子中含有2个氧原子 | |
| B. | Mg2+:一个镁原子带2个单位正电荷 | |
| C. | $\stackrel{+2}{Ca}$O氧化钙的化学价为+2价 | |
| D. | 2H:2个氢元素 |
4.小岳同学在复习气体的性质时,阅读到以下资料:制取气体的发生装置取决于反应前的药品状态和反应条件,收集气体的装置取决于气体能否与水反应、在水中的溶解性以及该气体相对于空气的密度大小.现有甲、乙、丙三种气体的反应前的物品状态、反应条件以及有关性质如下表,有关装置如下图.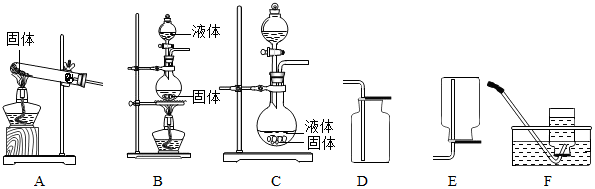
请你回答下列问题:
(1)能用发生装置A 制取的气体是乙(填“甲”、“乙”或“丙”);
(2)收集乙气体应选择的装置是E(填字母序号);
(3)实验室要制取和收集甲气体,请写出一个符合要求的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.

| 气体 | 反应前的药品状态 | 反应条件 | 气体性质 |
| 甲 | 固体+液体 | 常温 | 不与水反应,不易溶于水,密度比空气大 |
| 乙 | 固体+固体 | 加热 | 能与水发生反应,易溶于水,密度比空气小 |
| 丙 | 固体+液体 | 加热 | 能与水发生反应,能溶于水,密度比空气大 |
(1)能用发生装置A 制取的气体是乙(填“甲”、“乙”或“丙”);
(2)收集乙气体应选择的装置是E(填字母序号);
(3)实验室要制取和收集甲气体,请写出一个符合要求的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
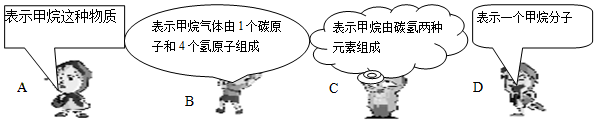
8. 如图为某物质的分子模型示意图,其中“
如图为某物质的分子模型示意图,其中“ ”代表氢原子,“
”代表氢原子,“ ”代表氧原子.下列有关叙述不正确的是( )
”代表氧原子.下列有关叙述不正确的是( )
 如图为某物质的分子模型示意图,其中“
如图为某物质的分子模型示意图,其中“ ”代表氢原子,“
”代表氢原子,“ ”代表氧原子.下列有关叙述不正确的是( )
”代表氧原子.下列有关叙述不正确的是( )| A. | 此物质属于化合物 | B. | 此物质中氧元素的化合价为-2价 | ||
| C. | 此物质的一个分子由4个原子构成 | D. | 此物质中氢氧元素的质量比是1:16 |
9.根据下表问题.
(1)60℃时,向两个分别盛有50g氯化钠和氯化铵的烧杯中,各加入100g的水.充分溶解后,达到饱和的是NaCl溶液.
(2)采用一种操作方法,将上述另一种未饱和的溶液变为饱和,下列说法正确的是CD(填字母序号,可多选).
A.溶液中溶质的质量一定增加 B.溶液中溶质的质量分数一定增大
C.溶液质量可能不变 D.可降低温度或增加溶质.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | 氯化钠 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| 氯化铵 | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 | |
(2)采用一种操作方法,将上述另一种未饱和的溶液变为饱和,下列说法正确的是CD(填字母序号,可多选).
A.溶液中溶质的质量一定增加 B.溶液中溶质的质量分数一定增大
C.溶液质量可能不变 D.可降低温度或增加溶质.
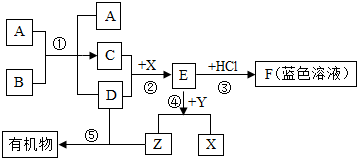 如图表示某些物质间转化关系(反应条件和部分产物已省略).其中A、E为金属氧化物,且均为黑色粉末;B、D是由相同元素组成的无色液体;且B具有消毒杀菌作用;C、Y、Z为无色气体,其中Y有毒;X是紫红色金属单质.
如图表示某些物质间转化关系(反应条件和部分产物已省略).其中A、E为金属氧化物,且均为黑色粉末;B、D是由相同元素组成的无色液体;且B具有消毒杀菌作用;C、Y、Z为无色气体,其中Y有毒;X是紫红色金属单质.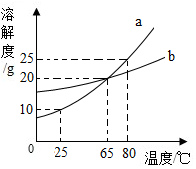 如图为a、b两物质的溶解度曲线,据图回答:
如图为a、b两物质的溶解度曲线,据图回答: