题目内容
5.写出下列化学符号或符号的意义:(1)氧元素O;(2)氦气He;(3)三个钙离子3Ca2+;(4)硫酸钾K2SO4;
(5)3CO23个二氧化碳分子;(6)Al3+铝离子;(7)正二价的钙$\stackrel{+2}{Ca}$;
(8)氧化镁中镁元素的化合价为+2$\stackrel{+2}{Mg}$O.
分析 本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
解答 解:(1)氧元素的元素符号为:O;
(2)氦是稀有气体元素,由稀有气体元素组成的单质是单原子分子,所以氦气的化学式就是表示氦元素的元素符号,即:He;
(3)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故三个钙离子可表示为:3Ca2+;
(4)硫酸钾是由显+1价的钾元素和显-2价的硫酸根组成,根据化合价原则,其化学式为:K2SO4;
(5)化学式前面加上数字表示几个这样的分子,故3CO2表示3个二氧化碳分子;
(6)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.故Al3+表示铝离子;
(7)元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以正二价的钙,故可表示为:$\stackrel{+2}{Ca}$;
(8)元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以氧化镁中镁元素的化合价为+2,故可表示为:$\stackrel{+2}{Mg}$O;
故答案为:(1)O;(2)He;(3)3Ca2+;(4)K2SO4;(5)3个二氧化碳分子;(6)铝离子;(7)$\stackrel{+2}{Ca}$;(8)$\stackrel{+2}{Mg}$O;
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.

| A. | 证明铁是金属活动性顺序表中氢之前的金属:2Fe+6HCl═2FeCl3+3H2↑ | |
| B. | 医疗上用氢氧化镁中和过多胃酸:Mg(OH)2+HCl═MgCl2+H2O | |
| C. | 实验室用高锰酸钾制取氧气:2KMnO4═K2MnO4+MnO2+O2 | |
| D. | 正常雨水pH约为5.6的原因:CO2+H2O═H2CO3 |
| A. | 煅烧后固体中钙元素的质量分数减少 | |
| B. | 共生成56g氧化钙 | |
| C. | 煅烧前后固体中氧元素的质量不变 | |
| D. | 共生成16g二氧化碳 |
| A. | 水变为水蒸气体积变大-分子间间隔增大 | |
| B. | 干冰升华-分子的体积变大 | |
| C. | 氧化汞受热分解-分子在化学变化中可以再分 | |
| D. | 闻到远处花香-分子在不断地运动 |
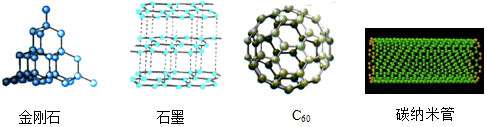
| A. | 在氧气中完全燃烧后的产物都是二氧化碳 | |
| B. | 原子的排列方式相同 | |
| C. | 它们的质地都很软 | |
| D. | 都有良好的导电性 |
| A. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | B. | H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | ||
| C. | 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 | D. | 2NaOH+CuSO4=Cu(OH)2↓+Na2SO4 |
| A. | 2g 碳酸钙高温分解产生的气体 | |
| B. | 2g 碳酸钙与足量盐酸充分反应产生的气体 | |
| C. | 0.24g碳在0.48g氧气中点燃产生的气体 | |
| D. | 0.24g碳与1.6g氧化铁混合物隔绝空气加强热,充分反应的气体 |
 根据所学溶液知识,解答下列问题:
根据所学溶液知识,解答下列问题:(1)如图是a、b、c三种固体物质(均不含结晶水)的溶解度曲线
①t1℃a、b、c的溶解度大小关系是b>a=c;
②t2℃将30克物质a加入到50克水中,形成溶液质量为75克;
③t2℃时,将a、b、c三种物质的饱和溶液降温至t1℃时,仍为饱和溶液的是a、b
④t2℃时,M点的a、b两种溶液质量分数大小关系为a等于b(填“大于”“小于”或“等于”)
(2)20℃时,将不同质量的NaCl晶体分别加入100g水中,充分溶解后所得溶液质量与加入NaCl晶体质量的对应关系如表:
| 组别 | A | B | C | D | E |
| NaCl晶体质量/g | 5 | 15 | 20 | 30 | 40 |
| 所得溶液质量/g | 105 | 115 | X | 130 | 136 |
(1)A组的溶液为不饱和(填“饱和”或“不饱和”)溶液.
(2)C组X的值为120g.