题目内容
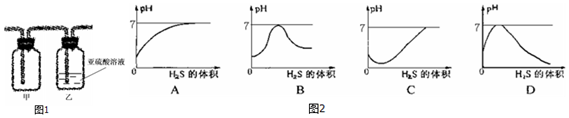
18.硫化氢(H2S)是一种具有臭鸡蛋气味的有毒气体,它的密度比空气大,可溶于水 形成氢硫酸,氢硫酸具有酸的通性,实验室常用固体硫化亚 铁(FeS)和稀硫酸在常温下制得,反应的化学方程式为 H2SO4+FeS=H2S↑+FeSO4.(1)实验室可以用图1所示的装置收集H2S气体,并对尾气进行处 理.尾气通入盛有饱和亚硫酸(H2SO3)溶液的洗气瓶,反应生成不溶于水的单质硫和水.写出尾气在乙瓶中反应的化学方程式:2H2S+H2SO3=3H2O+3S↓.
(2)在相同的条件下,氢硫酸的酸性比亚硫酸弱.则图2表示 乙瓶中溶液的 pH 随通入硫化氢体积的变化曲线示意图正确的是B
(3)实验室若制取 6.8克的硫化氢气体,理论上需要多少克固体硫化亚铁?
分析 (1)根据硫化氢和亚硫酸反应生成硫单质和水进行分析;
(2)根据题意,随着反应2H2S+H2SO3=3H2O+3S↓的发生会导致亚硫酸不断减少,溶液的酸性变弱,pH会不断变大,至恰好反应时pH等于7;继续滴加氢硫酸溶液,溶液显酸性,且酸性不断增强,pH会不断减小进行分析;
(3)根据硫化亚铁和硫酸反应生成硫酸亚铁和硫化氢,结合生成的硫化氢气体进行解答.
解答 解:(1)硫化氢和亚硫酸反应生成硫单质和水,化学方程式为:2H2S+H2SO3=3H2O+3S↓;
(2)酸性溶液pH小于7,且酸性越强pH越小.随着反应2H2S+H2SO3=3H2O+3S↓的发生,溶液的酸性变弱,pH会不断变大,图象会是一条上升的曲线;至恰好反应时pH等于7,继续滴加氢硫酸溶液会再次显酸性,但由于氢硫酸的酸性弱于亚硫酸,所以溶液最后的pH会比开始时大,故选:B;
(3)设理论上还需要硫化亚铁质量为x,
H2SO4+FeS=H2S↑+FeSO4
72 34
x 6.8g
$\frac{72}{x}=\frac{34}{6.8g}$
x=14.4g
故答案为:(1)2H2S+H2SO3=3H2O+3S↓;
(2)B;
(3)14.4g.
点评 本题是对物质发生化学反应时溶液pH的考查,解题的关键是对新信息读取、处理及对反应过程中溶液酸碱性的分析要到位,进而结合图象做出正确判断.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.在无色透明的酸性溶液中,能大量共存的一组离子是( )
| A. | NH4+、Al3+、SO42-、NO3- | B. | K+、Na+、OH-、Cl- | ||
| C. | K+、Mg2+、CO32-、SO42- | D. | Cu2+、Na+、SO42-、Cl- |
9.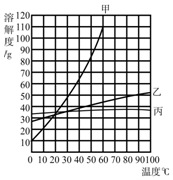 根据下列硝酸钾(KNO3)溶解度表和溶解度曲线图回答问题.
根据下列硝酸钾(KNO3)溶解度表和溶解度曲线图回答问题.
(1)图中硝酸钾(KNO3)的溶解度曲线是甲.
(2)60℃时,将甲、乙、丙的固体各40g分别加入100g水中充分溶解后,能形成饱和溶液的是丙.
(3)影响硝酸钾溶解度的因素是A.
A.温度B.压强C.水的质量
(4)现有大量的甲物质中混有少量的丙物质的混合物,要得到甲物质,可用降温结晶(填结晶的方法).
 根据下列硝酸钾(KNO3)溶解度表和溶解度曲线图回答问题.
根据下列硝酸钾(KNO3)溶解度表和溶解度曲线图回答问题.| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| KNO3溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
(2)60℃时,将甲、乙、丙的固体各40g分别加入100g水中充分溶解后,能形成饱和溶液的是丙.
(3)影响硝酸钾溶解度的因素是A.
A.温度B.压强C.水的质量
(4)现有大量的甲物质中混有少量的丙物质的混合物,要得到甲物质,可用降温结晶(填结晶的方法).
3.科学知识中有很多的“相等”,下列叙述错误的是( )
| A. | 参加化学反应的物质的总质量等于反应后生成的物质的总质量 | |
| B. | 同种元素的原子和离子的质子数相等 | |
| C. | MgO和NaOH中氧元素的质量分数相等 | |
| D. | 原子中原子核内的质子数和中子数一定相等 |
10.《三国演义》中有这样一个故事:诸葛亮率领的汉军误饮了“哑泉”.“哑泉,人若饮之,则不能言,不过旬晶必死”.后来,汉军将士经地方隐士指点,饮了万安溪的“安乐泉”水方才转危为安.“哑泉”和“安乐泉”中所含的化学物质可能分别是( )
| A. | NaCl、CaCl2 | B. | Na2SO4、BaCl2 | C. | FeCl3、NaOH | D. | CuSO4、Ca(OH)2 |
7.“遥知不是雪,为有暗香来”说明( )
| A. | 分子之间有间隔 | B. | 分子不断运动 | C. | 分子很小 | D. | 分子可分 |
8.下列物质的化学式和对应的俗称不一致的是( )
| A. | NaOH 烧碱 | B. | Ca(OH)2 熟石灰 | C. | Na2CO3 纯碱 | D. | NaCl 苛性钠 |