题目内容
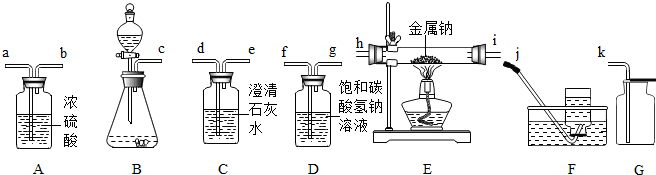
3.结合如图回答问题.
(1)实验室用甲装置制取二氧化碳,选择此装置的理由是反应为固液常温型、生成的气体密度比空气大且能溶于水.
(2)图乙中铜片上的白磷燃烧而红磷不燃烧,说明可燃物燃烧需要具备的条件是温度需达到着火点.本实验烧杯中热水是作用是使白磷达到着火点,而红磷不能达到着火点,且使水中的白磷与空气隔绝.
(3)图丙实验中有关反应的化学方程式为CO2+H2O═H2CO3,由该实验得出的结论是二氧化碳不能使石蕊变红,二氧化碳与水反应,生成碳酸,碳酸使石蕊变红(写出一条).
分析 (1)据二氧化碳的制取实验解答;
(2)根据燃烧的条件:具有可燃性,温度达到可燃物的着火点,与氧气接触,利用对比实验中的变量分析;
(3)二氧化碳与水反应生成碳酸.
解答 解:(1)二氧化碳的实验室制法是用稀盐酸与大理石(或石灰石.其主要成分都是碳酸钙)反应来制取,反应为固液常温型;
(2)白磷的着火点是40℃,红磷的着火点是240℃,薄铜片上的白磷燃烧而红磷不燃烧,说明物质燃烧,温度需要达到着火点;烧杯中热水的作用是:使白磷达到着火点,而红磷不能达到着火点,且使水中的白磷与空气隔绝;
(3)二氧化碳与水反应生成碳酸,反应的化学方程式为:CO2+H2O═H2CO3;以上实验说明二氧化碳不能使石蕊变红,二氧化碳与水反应,生成碳酸,碳酸使石蕊变红.
故答案为:(1)反应为固液常温型;(2)温度需达到着火点、使白磷达到着火点,而红磷不能达到着火点,且使水中的白磷与空气隔绝;(3)CO2+H2O═H2CO3、二氧化碳不能使石蕊变红,二氧化碳与水反应,生成碳酸,碳酸使石蕊变红.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
17.NaCl和KNO3在不同温度时的溶解度如表,试回答下列问题:
(1)20℃时,在50g水中溶解15.8gKNO3时,溶液恰好达到饱和状态;
(2)由海水中获取食盐通常采用“海水晒盐”方式获取食盐,由表中数据分析其原因是氯化钠的溶解度受温度影响变化不大;
(3)KNO3和NaCl在某一温度时具有相同的溶解度x,则x的取值范围是20-30℃;
(4)10℃时,分别将35gNaCl和KNO3固体加入100g水中,升温到60℃时,NaCl溶液为不饱和(填“饱和”或“不饱和”)溶液,升温前后有关溶液说法正确的是BC(填序号)
A.10℃时,两溶液中溶质质量分数相同
B.60℃时,两溶液中溶质质量分数相同
C.升温前后,NaCl溶液中溶质质量分数不变
D.升温前后,KNO3溶液中溶质质量分数不变.
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
(2)由海水中获取食盐通常采用“海水晒盐”方式获取食盐,由表中数据分析其原因是氯化钠的溶解度受温度影响变化不大;
(3)KNO3和NaCl在某一温度时具有相同的溶解度x,则x的取值范围是20-30℃;
(4)10℃时,分别将35gNaCl和KNO3固体加入100g水中,升温到60℃时,NaCl溶液为不饱和(填“饱和”或“不饱和”)溶液,升温前后有关溶液说法正确的是BC(填序号)
A.10℃时,两溶液中溶质质量分数相同
B.60℃时,两溶液中溶质质量分数相同
C.升温前后,NaCl溶液中溶质质量分数不变
D.升温前后,KNO3溶液中溶质质量分数不变.
18.下列说法正确的是( )
| A. | 碱中一定含有氢元素 | |
| B. | 物质都是由分子构成的 | |
| C. | 有盐和水生成的反应一定是中和反应 | |
| D. | 根据某元素的原子结构示意图可推断该元素原子核内的中子数 |
8. 全球近140个国家将在2020年前禁止生产和出口含汞产品,如荧光灯、化妆品、血压计等.关于汞元素的相关信息正确的是( )
全球近140个国家将在2020年前禁止生产和出口含汞产品,如荧光灯、化妆品、血压计等.关于汞元素的相关信息正确的是( )
 全球近140个国家将在2020年前禁止生产和出口含汞产品,如荧光灯、化妆品、血压计等.关于汞元素的相关信息正确的是( )
全球近140个国家将在2020年前禁止生产和出口含汞产品,如荧光灯、化妆品、血压计等.关于汞元素的相关信息正确的是( )| A. | 汞的化学式为Hg | B. | 汞原子的质量为200.6g | ||
| C. | 汞原子的中子数是80 | D. | 汞为非金属元素 |
 小乐发现切过咸菜的铁质菜刀很容易生锈,她猜测可能是咸菜中的盐水加快了铁的锈蚀,于是它设计了如图所示的实验:
小乐发现切过咸菜的铁质菜刀很容易生锈,她猜测可能是咸菜中的盐水加快了铁的锈蚀,于是它设计了如图所示的实验:

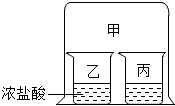 如图所示.小烧杯乙中盛有浓盐酸.在小烧杯丙中加入某种溶液后,立即用大烧杯甲罩住小烧杯乙和丙,烧杯丙中出现了明显变化.则烧杯丙中加入的溶液可能是B
如图所示.小烧杯乙中盛有浓盐酸.在小烧杯丙中加入某种溶液后,立即用大烧杯甲罩住小烧杯乙和丙,烧杯丙中出现了明显变化.则烧杯丙中加入的溶液可能是B