题目内容
12.推理是学习化学的一种重要方法,下列推理中,正确的是( )| A. | 某固体物质加入稀盐酸能产生气体,则该固体一定是“氢前”的金属 | |
| B. | 给水通直流电可以产生氢气和氧气,则水是由氢气和氧气组成的 | |
| C. | 溶液具有均一、稳定的特征,所以均一、稳定的物质一定是溶液 | |
| D. | 碱性溶液能使酚酞试液变红,则能使酚酞试液变红的一定是碱性溶液 |
分析 A、根据酸能与活泼金属、碳酸盐等反应生成气体进行分析判断;
B、根据电解水的实验结论、水的组成进行分析判断;
C、根据溶液特征进行分析判断;
D、无色酚酞溶液遇酸性溶液不变色,遇碱性溶液变红.
解答 解:A、某固体物质加入稀盐酸能产生气体,则该固体不一定是活泼金属,也可能是碳酸盐等,故选项说法错误;
B、给水通直流电可以产生氢气和氧气,氢气是由氢元素组成的,氧气是由氧元素组成的,则水是由氢元素和氧元素组成的,故选项说法错误;
C、溶液具有均一、稳定的特征,但均一、稳定的物质不一定是溶液,如水;故选项说法错误;
D、碱性溶液能使酚酞试液变红,则能使酚酞试液变红的一定是碱性溶液,故选项说法正确.
故选:D.
点评 本题难度不大,掌握酸的化学性质、水的组成、常见粒子的构成、常见酸碱指示剂的性质等是正确解答本题的关键.

练习册系列答案
相关题目
2.下列实验基本操作中,不正确的是( )
| A. | 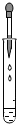 | B. | 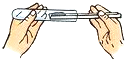 | C. |  | D. | 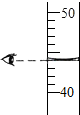 |
3.下列清洗方法中,利用乳化作用的是( )
| A. | 用自来水洗手 | B. | 用汽油清洗油污 | ||
| C. | 用食醋清洗茶壶水垢 | D. | 用洗涤剂清洗油腻的餐具 |
4.在一密闭容器中,有甲、乙、丙、丁四种物质,在一定的条件下,充分反应,测得反应前后各物质质量如下表:
关于此反应,下列认识正确的是( )
| 物 质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 4 | 18 | 10 | 1 |
| 反应后质量(g) | 待测 | 2 | 21 | 10 |
| A. | 该变化的基本反应类型是化合反应 | B. | 参加反应的甲、丙的质量比为2:11 | ||
| C. | 丙、丁是反应物 | D. | 甲反应后的质量为0g |
1.下列用途体现物质的物理性质的是( )
| A. | 生石灰可用来干燥过氧化氢溶液(又称双氧水)制得的氧气 | |
| B. | 打开浓盐酸的瓶盖,见到瓶口出现白雾现象 | |
| C. | 氢氧化钠不能用来治疗胃酸过多症 | |
| D. | 紫色石蕊遇到稀酸变为红色 |
2.人类的生产生活离不开金属,下列三种金属被发现、使用的先后顺序依次为铜、铁、铝.
(1)金属大规模被使用的先后顺序跟③(填序号)选项关系最大.
①地壳中金属元衷的含量 ②金属的导电性 ③金属的活动性
(2)为探究锰与铁的金属活动性,在相同温度下,取大小相同的两种金属薄片,用砂纸将表面擦光亮,分别投入等体积、等溶质质量分数的足量稀盐酸中反应,观察现象.请分析回答下列问题:
①两种金属投入盐酸前用砂纸将表面擦光亮,其主要目的是A.
A.除去氧化膜,便于直接反应 B.使表面不平整,易反应
C.表面光亮,易观察 D.提高金属温度,加快反应速度
②根据下表中的现象填写结论.
③除了比较与酸反应产生气体速率的快慢,你还有其他化学方法可比较这两种金属恬动性强弱吗?请举出一种方法(写出原理即可)FeSO4、Mn.
(3)将盛有等质量、等溶质质量分数的稀盐酸的两只烧杯,放在托盘天平左右两盘上,调节至平衡,再向两只烧杯中分别放入质量相等的镁和铁,待反应停止后,请判断:
①若天平仍保持平衡,烧杯中一定没有剩余的物质是稀盐酸.
②若天平失去平衡,则指针一定偏向放铁的一边.
(1)金属大规模被使用的先后顺序跟③(填序号)选项关系最大.
①地壳中金属元衷的含量 ②金属的导电性 ③金属的活动性
(2)为探究锰与铁的金属活动性,在相同温度下,取大小相同的两种金属薄片,用砂纸将表面擦光亮,分别投入等体积、等溶质质量分数的足量稀盐酸中反应,观察现象.请分析回答下列问题:
①两种金属投入盐酸前用砂纸将表面擦光亮,其主要目的是A.
A.除去氧化膜,便于直接反应 B.使表面不平整,易反应
C.表面光亮,易观察 D.提高金属温度,加快反应速度
②根据下表中的现象填写结论.
| 金属 | 铁 | 锰 |
| 与盐酸反应现象 | 放出气泡速度缓慢 | 放出气泡速度较快 |
| 结论 | 锰的金属活泼性大于铁. | |
(3)将盛有等质量、等溶质质量分数的稀盐酸的两只烧杯,放在托盘天平左右两盘上,调节至平衡,再向两只烧杯中分别放入质量相等的镁和铁,待反应停止后,请判断:
①若天平仍保持平衡,烧杯中一定没有剩余的物质是稀盐酸.
②若天平失去平衡,则指针一定偏向放铁的一边.
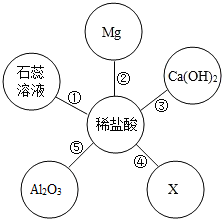 如图以稀盐酸为例的反应关系体现了酸的化学性质,其中X与图中所给物质的类别不同.结合此图回答下列问题:
如图以稀盐酸为例的反应关系体现了酸的化学性质,其中X与图中所给物质的类别不同.结合此图回答下列问题: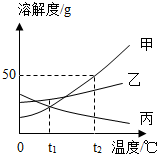 如图是甲、乙、丙三种固体物质在水中的溶解度曲线.
如图是甲、乙、丙三种固体物质在水中的溶解度曲线.