题目内容
17.如图分别是有关二氧化碳的制取、干燥,收集和性质检验的装置图.请回答下列问题: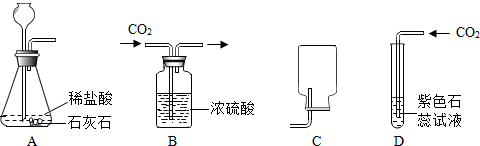
(1)请写出用装置A制取二氧化碳反应的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)四幅图中错误的是C;(填字母序号),如果实验室用装置A制取氧气,其反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)用D装置验证二氧化碳的性质时,反应现象是紫色石蕊试液变为红色.
分析 (1)根据实验室中制取二氧化碳的反应原理,进行分析解答.
(2)根据二氧化碳的密度比空气的大,应用向上排空气法收集,进行分析解答.
(3)根据二氧化碳与水反应生成碳酸,进行分析解答.
解答 解:(1)实验室中制取二氧化碳常用大理石或石灰石和稀盐酸反应来制取,同时生成氯化钙、水,反应的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)二氧化碳的密度比空气的大,应用向上排空气法收集,C图中瓶口向下,且导管没有伸入集气瓶的底部,装置错误.
如果实验室用装置A制取氧气,属于固液常温型,应采用分解过氧化氢溶液的方法,过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)二氧化碳与水反应生成碳酸,碳酸能使紫色石蕊溶液变红色,用D装置验证二氧化碳的性质时,反应现象是紫色石蕊试液变为红色.
故答案为:(1)CaCO3+2HCl=CaCl2+H2O+CO2↑; (2)C;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;(3)紫色石蕊试液变为红色.
点评 本题难度不大,是中考的重要考点之一,熟练掌握实验室中制取气体的反应原理、发生装置和收集装置的选择依据等是正确解答本题的关键.

练习册系列答案
相关题目
7.下列物质既是空气的成分,又属于氧化物的是( )
| A. | MgO | B. | H2O | C. | O2 | D. | 稀有气体 |
5.要除去下列各物质中的少量杂质,所选用的试剂或方法正确的是( )
| A. | Fe粉(CuO) 盐酸 | |
| B. | CO2(CO) 通过灼热的氧化铜 | |
| C. | Cu(Fe粉) 硝酸银溶液 | |
| D. | CO(CO2) 通入氧气 |
12. 小亮在实验室发现一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分只能看出溶质质量分数为10%.老师说,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙或碳酸
小亮在实验室发现一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分只能看出溶质质量分数为10%.老师说,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙或碳酸
钠中的一种.
(1)小亮查阅氢氧化钙常温下的溶解度为0.18g后,他认为该溶液不可能是氢氧化钙溶液,理由是常温下不可能得到质量分数为10%的氢氧化钙溶液.
(2)小亮用洁净干燥的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=10,他判断该溶液中不可能是氯化钠.对他的操作方法、测量结果及结论的评价,正确是B.
A.方法正确,结果正确,且结论正确 B.方法不正确,结果偏小,但结论正确
C.方法不正确,结果偏大,结论不正确 D.方法正确,结果正确,但结论不正确
(3)为了进一步确定该溶液的成分,小亮继续进行下列实验.
【设计实验方案】方案甲:选择氯化钡溶液来确定该溶液的成分;
方案乙:选择稀盐酸来确定该溶液的成分.
【进行实验】在两个方案中任选一个方案进行实验,填写步骤、现象、结论.
【实验反思】①有同学认为还可以用一种常见的碱溶液来确定是碳酸钠,它是Ca(OH)2溶液.有关反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
②小亮经过反思,向同学们提出如下建议,你认为不合理的是C.(填序号)
A.倾倒液体时应注意保护标签不被腐蚀
B.要有严谨的科学实验的态度
C.无法辨认的药品,直接倒掉,无需保留.
 小亮在实验室发现一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分只能看出溶质质量分数为10%.老师说,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙或碳酸
小亮在实验室发现一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分只能看出溶质质量分数为10%.老师说,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙或碳酸钠中的一种.
(1)小亮查阅氢氧化钙常温下的溶解度为0.18g后,他认为该溶液不可能是氢氧化钙溶液,理由是常温下不可能得到质量分数为10%的氢氧化钙溶液.
(2)小亮用洁净干燥的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=10,他判断该溶液中不可能是氯化钠.对他的操作方法、测量结果及结论的评价,正确是B.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管中,滴加稀硫酸溶液 氯化钡溶液 | 有气泡冒出, 出现白色沉淀 | 该溶液是碳酸钠溶液.反应方程式为: Na2CO3+H2SO4═Na2SO4+H2O+CO2↑ Na2CO3+BaCl2═2NaCl+BaCO3↓. |
C.方法不正确,结果偏大,结论不正确 D.方法正确,结果正确,但结论不正确
(3)为了进一步确定该溶液的成分,小亮继续进行下列实验.
【设计实验方案】方案甲:选择氯化钡溶液来确定该溶液的成分;
方案乙:选择稀盐酸来确定该溶液的成分.
【进行实验】在两个方案中任选一个方案进行实验,填写步骤、现象、结论.
【实验反思】①有同学认为还可以用一种常见的碱溶液来确定是碳酸钠,它是Ca(OH)2溶液.有关反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
②小亮经过反思,向同学们提出如下建议,你认为不合理的是C.(填序号)
A.倾倒液体时应注意保护标签不被腐蚀
B.要有严谨的科学实验的态度
C.无法辨认的药品,直接倒掉,无需保留.
9.2016年世界水日的宣传主题是“水与就业”,下列有关水的说法不正确的是( )
| A. | 含有冰的水也是纯净物 | |
| B. | 水电解所生成氢气和氧气的质量比是1:8 | |
| C. | 有水生成的反应不一定是酸和碱的中和反应 | |
| D. | 用明矾可以把硬水转化为软水 |
7.工业上需要大量的氧气,通常用分离液态空气的方法制取液态氧,然后汽化成氧气.下列说法不正确的是( )
| A. | 该过程为物理变化 | B. | 液氧变成氧气时氧分子的体积变大 | ||
| C. | 说明空气中含有氧气 | D. | 所得氧气能使带火星的木条复燃 |