题目内容
19.将ag锌粉和铜粉的混合物加到一定质量的AgNO3和Fe(NO3)2的混合溶液中,充分反应后过滤,得到滤渣和滤液,下列有关说法正确的是( )| A. | 若滤渣质量小于ag,滤液一定是无色的 | |
| B. | 若滤渣质量小于ag,滤渣中一定有Fe、Cu、Ag | |
| C. | 若滤渣质量大于ag,滤液中一定没有Ag+ | |
| D. | 若滤渣质量大于ag,滤渣中一定没有Fe |
分析 在金属活动性顺序表中,位于前面的金属能把位于后面的金属从其盐溶液中置换出来及其反应的质量关系分析判断即可.
解答 解:由于金属的活动性顺序是锌>铁>铜>银,将锌粉和铜粉的混合物加到一定质量的AgNO3和Fe(NO3)2的混合溶液中,锌先与硝酸银反应生成了硝酸锌和银,当硝酸银反应完成后锌与硝酸亚铁反应生成了硝酸锌与铁,若有剩余硝酸银,铜能硝酸银反应生成了硝酸铜和银.反应的质量关系是:
Zn+2AgNO3═Zn(NO3)2+2Ag
65 216
Zn+Fe(NO3)2=Zn(NO3)2+Fe
65 56
Cu+2AgNO3═Cu(NO3)2+2Ag
64 216
由于锌硝酸银反应滤渣的质量增加,锌与硝酸亚铁反应反应滤渣的质量减少,若滤渣质量小于ag,说明锌一定与硝酸亚铁发生了反应,铜没有发生反应;若滤渣质量大于ag,锌可能与硝酸亚铁发生了反应.
A、若滤渣质量小于ag,不能确定溶液中的硝酸亚铁是否完全反应,滤液不一定是无色的,故A错误;
B、由上述反应可知,若滤渣质量小于ag,滤渣中一定有Fe、Cu、Ag,故B正确;
C、若滤渣质量大于ag,不能确定溶液中的硝酸硝酸银是否完全反应,滤液中可能Ag+,故C错误;
D、若滤渣质量大于ag,滤渣中可能少量的Fe,故D错误.
故选:B.
点评 本题考查了金属活动性顺序的应用,完成此题可以依据金属活动性顺序的及其反应的质量关系进行分析判断.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
10.某化学兴趣小组为测定某有机物(含C、H、O三种元素)中各元素的质量比,用如图实验装置(部分夹持装置略去)进行探究.
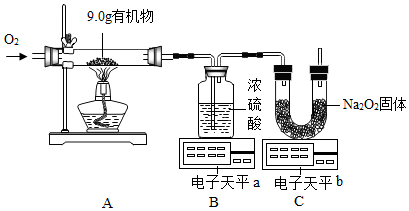
提示:装置C中发生的反应为2Na2O2+2CO2=2Na2CO3+O2
实验数据:
请计算该有机物中各元素的质量比(写出计算过程).

提示:装置C中发生的反应为2Na2O2+2CO2=2Na2CO3+O2
实验数据:
| 读数 | 反应前质量/g | 反应后质量/g |
| 电子天平a | 217.0 | 222.4 |
| 电子天平b | 150.0 | 158.4 |
14.近代发明联合制碱法的科学家是( )
| A. |  侯德榜 | B. |  拉瓦锡 | C. |  门捷列夫 | D. |  道尔顿 |
4.下列物品的主要材料,属于有机合成材料的是( )
| A. |  不锈钢餐具 | B. |  纯棉毛巾 | C. |  玻璃杯 | D. |  塑料筐 |
11.下列实验操作与实验目的相对应的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 除去CuSO4溶液中的少量FeSO4 | 加入足量的铁粉,过滤 |
| B | 除去CO2中的HCl气体 | 通入足量的氢氧化钠溶液中 |
| C | 除去MnO2中的KCl | 加入足量的水,溶解,过滤、干燥 |
| D | 除去KCl中的少量K2CO3 | 加入足量的稀硫酸,蒸发结晶 |
| A. | A | B. | B | C. | C | D. | D |
8.下列各组离子在水中一定能大量共存,并形成无色透明溶液的是( )
| A. | Ba2+、Cu2+、SO42-、H+ | B. | H+、Ca2+、CO32-、Mg+ | ||
| C. | Fe2+、Cl-、NO3-、K+ | D. | Na+、OH-、Cl-、Ba2+ |
9.2017年中国环境日的主题是“绿水青山就是金山银山”,倡导人们自觉践行绿色生活,共同建设美丽中国.下列做法符合这一主题的是( )
| A. | 大力发展燃煤发电 | B. | 鼓励国民自驾出行 | ||
| C. | 推广使用清洁能源 | D. | 大量开采矿产资源 |