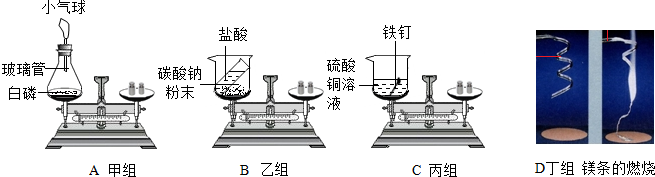
题目内容
金属的生产和使用是人类文明和社会进步的一个重要标志.每年世界上钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失.
(1)铁在空气中锈蚀,实际上是铁跟 等物质相互作用的结果.
(2)防止钢铁锈蚀的方法 ;
(3)工人师傅在焊接钢铁制品时,通常先用稀盐酸除去钢铁表面上的铁锈,反应化学方程式为 .
(4)金属的回收和利用是保护金属资源的一种有效途径.废钢铁可回收重新冶炼,用一氧化碳还原氧化铁的化学方程式为 ;
(5)查阅资料:金属在活动性顺序里的位置越后,其构成化合物越不稳定,它的氧化物在高温条件下可以被活动性强的金属还原成金属单质.请你选择一组能发生化学反应的药品
(①铝和氧化铁②铁和氧化铝)写出该反应的化学方程式 .
(1)铁在空气中锈蚀,实际上是铁跟
(2)防止钢铁锈蚀的方法
(3)工人师傅在焊接钢铁制品时,通常先用稀盐酸除去钢铁表面上的铁锈,反应化学方程式为
(4)金属的回收和利用是保护金属资源的一种有效途径.废钢铁可回收重新冶炼,用一氧化碳还原氧化铁的化学方程式为
(5)查阅资料:金属在活动性顺序里的位置越后,其构成化合物越不稳定,它的氧化物在高温条件下可以被活动性强的金属还原成金属单质.请你选择一组能发生化学反应的药品
(①铝和氧化铁②铁和氧化铝)写出该反应的化学方程式
考点:金属锈蚀的条件及其防护,铁的冶炼,酸的化学性质,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)根据金属生锈的知识进行分析,铁在有水和氧气并存时易生锈解答;
(2)根据要防锈就是使铁与水和氧气隔绝解答;
(3)根据盐酸能与钢铁制品表面的锈氧化铁反应生成氯化铁和水解答;
(4)根据一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳解答;
(5)根据铝和氧化铁在高温时发生反应,生成铁和氧化铝,写出该反应的化学方程式.
(2)根据要防锈就是使铁与水和氧气隔绝解答;
(3)根据盐酸能与钢铁制品表面的锈氧化铁反应生成氯化铁和水解答;
(4)根据一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳解答;
(5)根据铝和氧化铁在高温时发生反应,生成铁和氧化铝,写出该反应的化学方程式.
解答:解:
(1)铁在有水和氧气并存时易生锈,所以本题答案为:水,氧气;
(2)要防锈就是使铁与水和氧气隔绝,可以采取覆盖保护层的方法,所以本题答案为:涂油,刷油漆;
(3)盐酸能与钢铁制品表面的锈氧化铁反应生成氯化铁和水,所以本题答案为:Fe2O3+6HCl═2FeCl3+3H2O;
(4)一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,化学方程式为:Fe2O3+3CO
2Fe+3CO2
(5)铝和氧化铁在高温时发生反应,生成铁和氧化铝,该反应的化学方程式为:2Al+Fe2O3
2Fe+Al2O3
答案:
(1)水,氧气
(2)涂油,刷油漆
(3)Fe2O3+6HCl═2FeCl3+3H2O
(4)Fe2O3+3CO
2Fe+3CO2
(5)2Al+Fe2O3
2Fe+Al2O3
(1)铁在有水和氧气并存时易生锈,所以本题答案为:水,氧气;
(2)要防锈就是使铁与水和氧气隔绝,可以采取覆盖保护层的方法,所以本题答案为:涂油,刷油漆;
(3)盐酸能与钢铁制品表面的锈氧化铁反应生成氯化铁和水,所以本题答案为:Fe2O3+6HCl═2FeCl3+3H2O;
(4)一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,化学方程式为:Fe2O3+3CO
| ||
(5)铝和氧化铁在高温时发生反应,生成铁和氧化铝,该反应的化学方程式为:2Al+Fe2O3
| ||
答案:
(1)水,氧气
(2)涂油,刷油漆
(3)Fe2O3+6HCl═2FeCl3+3H2O
(4)Fe2O3+3CO
| ||
(5)2Al+Fe2O3
| ||
点评:本题考查了铁生锈的知识及其防治,完成此题,可以依据已有的知识进行.

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
下列生活中的变化,涉及化学变化的是( )
| A、碾米 | B、淘米 | C、洗菜 | D、酿酒 |
下列各组物质的稀溶液,不用其他试剂就能鉴别出来的是( )
| A、FeCl3、NaOH、Na2SO4、KCl |
| B、Na2CO3、HCl、CaCl2、HNO3 |
| C、NH4Cl、KOH、Na2SO4、BaCl2 |
| D、KNO3、HCl、NaOH、FeCl3 |
向硫酸亚铁.硫酸铜的混合溶液中加入一些锌粉,充分反应后过滤,得到固体不溶物A和滤液,则A的组成不可能是( )
| A、只含有Zn.Cu |
| B、只含有 Fe.Cu |
| C、含有Zn.Fe.Cu |
| D、只含有Cu |
化学与医学密切相关,以下有关医疗的化学问题错误的是( )
| A、0.9%的生理盐水是指溶质与溶液的质量比为0.9:100 |
| B、氧气可用于急救 |
| C、烧碱可用于治疗胃酸过多 |
| D、钛合金与人体具有很好的相溶性,可用于制人造骨 |
在Cu(NO3)2和AgNO3的混合溶液里加入一定量的铁粉并充分振荡,待反应完毕后过滤.以下对实验结果的分析推理中不正确的是( )
| A、若滤渣中只有银时,滤液中一定有Cu2+、Fe2+ |
| B、若滤渣中有银、铜时,滤液中一定有Fe2+,可能有Cu2+ |
| C、若滤渣中有银、铜时,滤液中一定有Fe2+,可能有Ag+ |
| D、若滤渣中有银、铜、铁时,滤液中一定有Fe2+ |
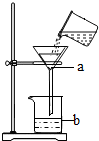 如图为某学生在做粗盐提纯时,过滤操作的示意图:
如图为某学生在做粗盐提纯时,过滤操作的示意图: