题目内容
7.甲、乙两个实验小组分别进行“Na2CO3和N aCl混合物中Na2CO3含量测定”的实验:
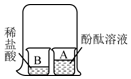
(1)甲的方法是:利用如图实验装置,将一定质量的样品与足量稀盐酸反应,测定反应后生成CO2的体积,再计算出样品中Na2CO3的质量.
①为了准确测量反应生成二氧化碳的体积,应在A开始用量筒收集气体.
A、实验开始时 B有连续气泡产生时 C先用燃着的木条检验熄灭后
②如果读数时,量筒中的液面高于水槽中的液面,测出的二氧化碳的体积将偏偏大.
(2)乙组的方法是:取20克样品,加水溶解后逐渐滴加溶质质量分数为7.3%的稀盐酸,反应过程中不断搅拌,测量溶液的pH和对应的滴入盐酸质量,记下三组数据(如表),请计算样品中Na2CO3质量分数.(不考虑二氧化碳在水中的溶解)
| 实验次序 | 1 | 2 | 3 |
| 溶液的pH | 8 | 7 | 6 |
| 对应的滴入盐酸质量 | 37 | 40 | 43 |
分析 (1)①根据碳酸钠与盐酸反应有二氧化碳气体生成分析回答;
②根据气体的压强与体积的关系分析.
(2)根据结合图2中数据,分析恰好反应时滴入的盐酸的质量,求出碳酸钠的质量,再求出样品中Na2CO3的质量分数
解答 解:(1)①由于碳酸钠与盐酸反应有二氧化碳气体生成,应在实验开始时开始用量筒收集气体;
②如果读数时,量筒中的液面高于水槽中的液面,量筒内的压强偏小,则测出的二氧化碳的体积将偏大;
(2)由结合图2中数据可住,恰好反应时滴入的盐酸的质量是40g,
设样品中Na2CO3的质量为x
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73
x 40g×3.65%
$\frac{106}{73}$=$\frac{x}{40g×3.65%}$
解得 x=2.12g
样品中Na2CO3的含量是$\frac{2.12g}{20g}$×100%=10.6%
答案:(1)①A,②A;(2)样品中Na2CO3的质量分数是10.6%.
点评 本题主要考查测定混合物中某种成分含量方面的知识,解答本题要从物质的性质方面进行分析、判断,从而得出正确的结论.此题是一道实验综合题,涉及到实验的基本操作和根据化学方程式的计算,.

练习册系列答案
相关题目
6.下列有关微粒的说法正确的是( )
| A. | 分子可以再分,而原子不能再分 | B. | 分子大,原子小 | ||
| C. | 原子失去电子变成阴离子 | D. | 分子、原子、离子都可以构成物质 |
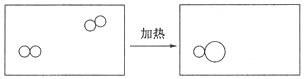
2.如图是某化学反应的示意“ ”与“
”与“ ”图(代表不同种元素原子),有关该反应下列说法正确的是( )
”图(代表不同种元素原子),有关该反应下列说法正确的是( )
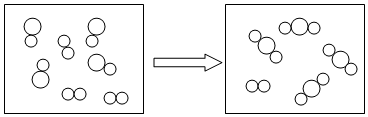
 ”与“
”与“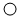 ”图(代表不同种元素原子),有关该反应下列说法正确的是( )
”图(代表不同种元素原子),有关该反应下列说法正确的是( )
| A. | 该反应为置换反应 | B. | 反应后得到的物质为混合物 | ||
| C. | 参加反应的分子个数比为3:4 | D. | 该反应可能是4CO+2O2$\frac{\underline{\;点燃\;}}{\;}$4CO2 |
12.下列食品用于补钙效果较好的是( )
| A. |  白糖 | B. |  大米 | C. |  肥肉 | D. |  奶和奶制品 |
19.如图所示实验操作中不正确的是( )
| A. | 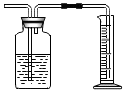 排水法测量气体的体积 | B. | 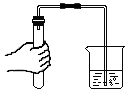 检查装置气密性 | ||
| C. |  滴管用完即插回 | D. | 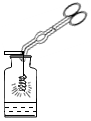 铁丝在氧气中燃烧 |
17.在《超人》这部美国漫画中,主角超人虽然有超能力,但是氪石却是他的“天敌”.令人意外的是,英国科学家在西伯利亚发现了一种新矿石,它的化学结构与《超人》中来自外太空的氪晶体基本相同.然而,与之不同的是,真实的氪矿石并非大块绿色晶体,而是白色粉末状物质,而且它不含氟,不具有辐射性.下列有关说法正确的是( )
| A. | 漫画中的氪矿石中所含的氟指的是氟元素 | |
| B. | 真实的氪矿石不会熔化 | |
| C. | “白色”是真实的氪矿石的一种化学性质 | |
| D. | 漫画中的氪矿石属于单质 |
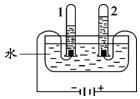 水和溶液在生产、生活中起着十分重要的作用.
水和溶液在生产、生活中起着十分重要的作用.