题目内容
8.某实验小组在探究物质性质实验时,做了如图所示的三个实验
(1)实验一:氢氧燃料电池的示意图,电池在工作时,H2和O2反应生成水,同时提供电能,溶液的pH变小(选填“变大”、“不变”或“变小”)
(2)实验二:装置②中的小试管外壁贴有4片试纸,可以利用上述装置验证二氧化碳的性质.实验时装置①所发生的反应方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑;该实验能够证明二氧化碳具有的化学性质是能与水反应生成碳酸.
(3)实验三:实验中观察到玻璃管内固体由红棕色变为黑色,说明气体X具有还原性,Fe2O3具有氧化性.
分析 (1)电池工作时氢气与氧气生成水使溶液中氢氧化钾的溶质质量分数变小,碱性减弱据此分析回答.
(2)根据实验室制取二氧化碳的反应原理书写方程式;根据现象和二氧化碳的性质分析解答;
(3)根据氧化铁在反应中的变化来分析.
解答 解:(1)电池工作时氢气与氧气生成水使溶液中氢氧化钾的溶质质量分数变小,碱性减弱,溶液的pH会变小;故填:变小;
(2)实验室制取二氧化碳用的药品是大理石或石灰石和稀盐酸,反应生成氯化钙、水和二氧化碳;酸性溶液可使石蕊试液变红,根据题意:装置中小试管外壁贴有4片试纸:其中两端的两片用紫色石蕊溶液润湿,中间两片用紫色石蕊溶液浸过并晒干.将制得的干燥的二氧化碳气体缓缓流入小试管内,将会观察到:干燥试纸无变化,湿润试纸由下而上依次变红,说明二氧化碳密度比空气大,所以下边的先变红,二氧化碳本身不能使石蕊变红,故干燥的试纸未变色,润湿的试纸变红说明二氧化碳与水反应生成酸性物质;故填:CaCO3+2HCl=CaCl2+H2O+CO2↑;能与水反应生成碳酸;
(3)实验中观察到玻璃管内固体由红棕色变为黑色,这说明氧化铁被X还原为铁,氧化铁失去氧变成了铁,这说明了氧化铁发生了还原反应,被X还原,本身具有氧化性,在反应中充当氧化剂;故填:氧化.
点评 熟悉燃料电池的工作原理、溶液酸碱性与酸碱度的关系、二氧化碳的实验室制取方法与性质、氧化还原反应的知识是解题的关键.

练习册系列答案
相关题目
19.随着我国载人航天技术的发展,我国已成为世界上第三个成功载人登上太空的国家,将“神舟九号”飞船送入太空的是“长征二号”F运载火箭,火箭工作中发生的反应为:C2H8N2+2R═3N2+2CO2+4H2O,则R的化学式为( )
| A. | NO | B. | NO2 | C. | N2O4 | D. | HNO3 |
3.下列4个图象分别代表对应的4种过程,其中不正确的是( )
 |  | 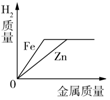 | 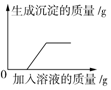 |
| A、向饱和石灰水中加入少量生石灰固体 | B、向含有HCl的CaCl2溶液中滴加Na2CO3溶液 | C、向等质量、等浓度的稀硫酸中分别加入过量的Zn和Fe | D、向HCl和CuSO4的混合溶液中加入过量的Ba(OH)2溶液 |
| A. | A | B. | B | C. | C | D. | D |
13.只用一种试剂就能鉴别出Na2CO3、BaCl2、NaCl三种溶液,这种试剂是( )
| A. | NaOH | B. | AgNO3 | C. | H2SO4 | D. | CaCl2 |
20.将铁粉和镁粉的混合物 ag 加入 Cu(NO3)2溶液中,反应结束后,过滤.下列对滤渣成分的说明中,正确的是( )
| A. | 滤渣的质量一定大于 ag | B. | 滤液一定不是无色的 | ||
| C. | 滤渣中一定有单质铜和单质铁 | D. | 滤液中至少含有两种金属阳离子 |
6.下列描述中,属于氧气化学性质的是( )
| A. | 通常状况下,氧气是无色、无味的气体 | |
| B. | 通过低温加压,可以使氧气液化成淡蓝色的液体 | |
| C. | 氧气不易溶于水 | |
| D. | 氧气是一种性质比较活泼的气体,能与许多物质发生氧化反应 |