题目内容
7.下列物质露置在空气中因变质而导致溶液的总质量增加的是( )| A. | 氢氧化钠溶液 | B. | 浓盐酸 | C. | 浓硫酸 | D. | 氯化钠溶液 |
分析 敞口瓶久置于空气发生变质即发生了化学变化,也就是与空气中的成分发生了化学反应,生成了新的物质,根据常见物质的化学性质进行分析判断.
解答 解:A、氢氧化钠溶液长期放置在空气中能与二氧化碳发生反应生成碳酸钠和水,发生变质且质量增加,故选项正确.
B、浓盐酸具有挥发性,长期放置在空气中质量会减小,在挥发过程中没有发生化学变化,没有变质,故选项错误.
C、浓硫酸具有吸水性,长期放置在空气中质量会增加,在吸水过程中没有发生化学变化,没有变质,故选项错误.
D、氯化钠溶液不和空气中物质反应,不会发生变质,质量不变,故选项错误.
故选:A.
点评 本题难度不大,掌握常见的酸碱盐的性质、在空气中的质量变化等是正确解答此类题的关键.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
19.如图所示是实验过程中的部分操作,其中正确的是( )
| A. | 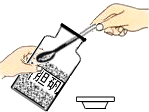 取一定量粗盐 取一定量粗盐 | B. | 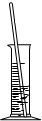 溶解 | C. | 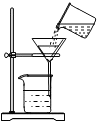 过滤 | D. |  蒸发结晶 |
15. 已知氯化钾和硝酸钾在不同温度时的溶解度如表所示:
已知氯化钾和硝酸钾在不同温度时的溶解度如表所示:
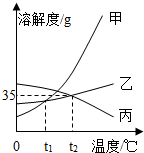
(1)依据表格数据,绘制出氯化钾和硝酸钾的溶解度曲线如图所示,图中能表示硝酸钾的溶解度曲线的是甲(选填“甲”或“乙”).
(2)t2℃时,丙物质的溶解度为35g.现有该温度下接近饱和的丙物质的溶液,使其变成饱和溶液,可采用的方法有加入丙(或恒温蒸发溶剂).
(3)40℃时,将30g氯化钾放入盛有50g水的烧杯中,充分溶解后,所得溶液的质量为70g.此时,该溶液的溶质质量分数为28.6%(结果精确到0.1%).若将烧杯内的物质降温到20℃,溶液中不变的是B(填写序号)
A、溶质的质量 B、溶剂的质量 C、溶液的质量 D、溶质质量分数.
 已知氯化钾和硝酸钾在不同温度时的溶解度如表所示:
已知氯化钾和硝酸钾在不同温度时的溶解度如表所示:| 温度/℃ | 0 | 20 | 40 | 60 | |
| 溶解度/g | 氯化钾 | 27.6 | 34.0 | 40.0 | 45.5 |
| 硝酸钾 | 13.3 | 31.6 | 63.9 | 110.0 | |
(2)t2℃时,丙物质的溶解度为35g.现有该温度下接近饱和的丙物质的溶液,使其变成饱和溶液,可采用的方法有加入丙(或恒温蒸发溶剂).
(3)40℃时,将30g氯化钾放入盛有50g水的烧杯中,充分溶解后,所得溶液的质量为70g.此时,该溶液的溶质质量分数为28.6%(结果精确到0.1%).若将烧杯内的物质降温到20℃,溶液中不变的是B(填写序号)
A、溶质的质量 B、溶剂的质量 C、溶液的质量 D、溶质质量分数.
2.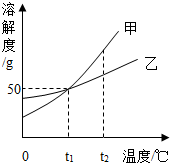 如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的是( )
如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的是( )
 如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的是( )
如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的是( )| A. | t1℃时,甲、乙两种物质的溶解度都是50g | |
| B. | t2℃时,在等质量甲、乙两种溶液中,甲中溶质的质量一定大于乙 | |
| C. | t1℃时,将甲、乙的饱和溶液升温至t2℃,二者溶质的质量分数相等 | |
| D. | 甲溶液中含有少量乙,可以用冷却热饱和溶液的方法提纯甲 |
16.下列变化中前者属于是化学变化,后者属于物理变化的是( )
| A. | 瓦斯爆炸,煤的干馏 | B. | 呼吸作用,食物腐烂 | ||
| C. | 海水晒盐,西瓜榨汁 | D. | 烧制瓷器,石油分馏 |
17.小强和小明两位同学在实验室用下列装置制取几种气体.

(1)写出图中有标号仪器的名称:a是长颈漏斗,b是水槽.
(2)小强想用高锰酸钾制取一瓶氧气应选用的发生装置是A(填装置序号),而小明认为该装置有一个小问题,请你帮助他:试管口放一团棉花;实验室用该方法制取氧气的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)在装入药品前,应先进行的一项操作是检验装置的气密性.
(4)小明要制取少量CO2,其反应原理是CaCO3+2HCl=CaCl2+CO2↑+H2O(用化学方程式表示),他收集该气体的装置是(填装置序号)D,选用该装置的理由是.
(5)为了防止生成的气体从C装置仪器a逸出,必须使a仪器下端管口伸入液面以下.
(6)小强和小明还对过氧化氢分解时影响反应速率的部分因素作出探究,并测得相关实验数据.如下表:
从实验③和④对比可知,化学反应速率与温度有关.通过实验①与②对比可知,化学反应速率与反应物的有关.若用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,加适量水稀释,产生氧气的总质量不变.(选填“减小”或“不变”或“增大”).

(1)写出图中有标号仪器的名称:a是长颈漏斗,b是水槽.
(2)小强想用高锰酸钾制取一瓶氧气应选用的发生装置是A(填装置序号),而小明认为该装置有一个小问题,请你帮助他:试管口放一团棉花;实验室用该方法制取氧气的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)在装入药品前,应先进行的一项操作是检验装置的气密性.
(4)小明要制取少量CO2,其反应原理是CaCO3+2HCl=CaCl2+CO2↑+H2O(用化学方程式表示),他收集该气体的装置是(填装置序号)D,选用该装置的理由是.
(5)为了防止生成的气体从C装置仪器a逸出,必须使a仪器下端管口伸入液面以下.
(6)小强和小明还对过氧化氢分解时影响反应速率的部分因素作出探究,并测得相关实验数据.如下表:
| 实验序号 | H2O2溶液浓度% | H2O2溶液体积/mL | 温度/℃ | MnO2的用量/g | 收集氧气的体积/mL(排水法) | 反应所需时间/s |
| ① | 5 | 1 | 20 | 0.1 | 2 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 2 | 12.63 |
| ③ | 20 | 5 | 25 | 0.2 | 4 | 10.70 |
| ④ | 20 | 5 | 35 | 0.2 | 4 | 8.06 |
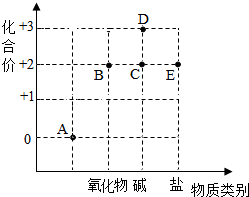 以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图.如图为铁的价类图,例如E点可表示+2价的亚铁盐.请回答:
以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图.如图为铁的价类图,例如E点可表示+2价的亚铁盐.请回答: