题目内容
17.现有如图1仪器或装置,请回答下列问题: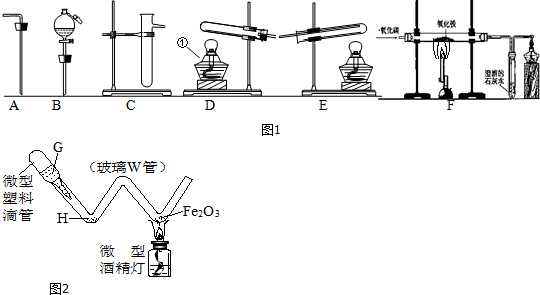
Ⅰ、(1)仪器①的名称酒精灯;实验室用一氧化碳还原氧化铁的实验可选装置F(填字母),反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)草酸(H2C2O4) 固体在浓硫酸作用下发生反应:H2C2O4═CO2↑+CO↑+H2O,若用该反应来制取CO,制气装置应选B、C(填字母);除去其中的CO2可选仪器A和C,C中装入的试剂最好是a(填小写字母):
a.烧碱溶液 b.浓硫酸 c.澄清石灰水 反应方程式为:CO2+2NaOH=Na2CO3+H2O.
Ⅱ、如图2为某种“微型”实验装置.如果G处装稀盐酸,H处放少量铁屑,则加热处的现象为固体粉末由红色逐渐变黑;“微型塑料滴管”相当于图1实验装置中的B(填字母);用微型仪器进行实验,除试剂用量极少以外,还可能具有的优点是操作简单;可控制反应中的速率;减少废弃物质或有害物质的排放量 (任写一点)
分析 Ⅰ、熟记仪器名称,根据一氧化碳还原氧化铁的反应特点,判断所应选用的装置,并完成反应的化学方程式;
根据制取CO的反应中所使用药品状态及反应的条件,选择合适的仪器组成制取该气体的发生装置,根据二氧化碳的化学性质,选择可除去二氧化碳气体的试剂,写出除去二氧化碳的反应的化学方程式;
Ⅱ、“微型塑料滴管”G的稀盐酸流入H处与铁屑接触,产生氢气;氢气与氧化亚铁反应,描述该反应出现的现象,分析装置的特点.
解答 解:Ⅰ、(1)仪器①为用于加热的仪器酒精灯;为实现CO还原氧化铁且检验反应生成的气体及尾气处理,应选择装置F完成还原氧化铁的实验,该反应的化学方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;故填:酒精灯,F,3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)制取CO时使用了草酸(H2C2O4) 固体在浓硫酸作用下发生反应,因此可选择BC两种仪器组装成制取气体的装置;为除去混在CO中的二氧化碳气体,可把混合气体通过氢氧化钠溶液,使二氧化碳被氢氧化钠溶液所吸收,反应的化学方程式为CO2+2NaOH=Na2CO3+H2O.
故填:B、C,a,CO2+2NaOH=Na2CO3+H2O,
Ⅱ、生成的氢气与氧化亚铁反应生成铁和水,因此可观察到固体粉末逐渐变黑;微型塑料滴管在装置中起到加入液体药品且可以控制液体的流速的作用,与图中装置B的作用相似;用微型仪器进行实验,除试剂用量极少以外,还可能具有的优点是:产生废物少(或污染少、或加热需要的热量少、或反应时间短).
故填:固体粉末由红色逐渐变黑,B,操作简单;可控制反应中的速率;减少废弃物质或有害物质的排放量(其它合理答案也给)
点评 本题综合考查了铁的冶炼、反应发生装置的选用、化学方程式的书写等基础知识,解答时应沉稳对待.

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案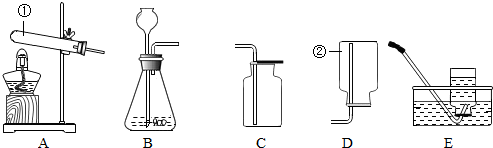
(1)写出装置图中标号仪器的名称:①试管;②集气瓶.
(2)写出该反应的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,选择的发生装置是B(填编号),不能用D收集的原因是氧气密度大于空气.
(3)小刚同学查资料得知氧化铁也可以加快双氧水分解速度,他们进行了以下实验探究:
①往盛有5mL 5%H2O2溶液的试管中,伸入带火星的木条,木条不复燃.
②往盛有5mL w%H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃.
③经检验,②中反应后试管中仍含有a g Fe2O3
问题:①Fe2O3在上述反应中(是、否)是催化剂.②中H2O2的浓度(W%)以5%为宜.
(4)研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究.下表选取了部分实验数据:
用足量等体积H2O2溶液制取相同体积O2所需的时间.
时间(min) 浓度 条件 | 30% H2O2 | 15%H2O2 | 5%H2O2 |
| 加入a g MnO2 | 0.2 | 0.8 | 2.0 |
| 加入a g Fe2O3 | 7.0 | 9.0 | 16.0 |
| A. | 混合物可能是由一种元素组成的物质 | |
| B. | 氧气具有可燃性,是一种常见的燃料 | |
| C. | 氧气能与许多物质发生氧化反应,是一种典型的氧化物 | |
| D. | 催化剂一定能加快化学反应速率,但不能改变生成物的量 |
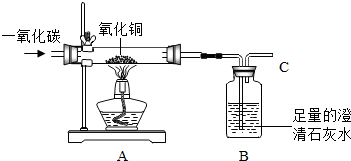 CO是一种无色、无味、有毒的可燃气体污染物,具有还原性,可用于冶金工业.某兴趣小组为探究其具有还原性,设计了右图实验装置.请回答以下有关问题:
CO是一种无色、无味、有毒的可燃气体污染物,具有还原性,可用于冶金工业.某兴趣小组为探究其具有还原性,设计了右图实验装置.请回答以下有关问题:
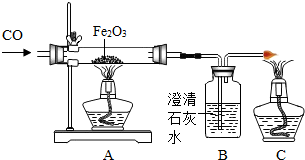 如图为实验室研究炼铁的化学原理的装置,请回答与该实验有关的问题.
如图为实验室研究炼铁的化学原理的装置,请回答与该实验有关的问题.