题目内容
19.在实验室加热30g氯酸钾和二氧化锰混合物制取氧气,加热至不再产生气体为止,称量剩余固体质量为20.4g.请计算:
(1)生成氧气的质量为9.6g.
(2)固体剩余物中氯化钾的质量.
(3)回收固体混合物中的MnO2的步骤:溶解、过滤、洗涤、干燥.
分析 根据质量守恒定律可知试管内物质质量的减少量就是生成的氧气的质量,根据方程式由氧气的质量,列比例式计算出参加反应的氯酸钾和氯化钾的质量即可,MnO2不溶于水,KCl溶于水,以此来解答.
解答 解:(1)由于是完全反应,根据质量守恒,减少的质量就是生成的氧气的质量,即制得氧气:30g-20.4g=9.6g;
故填:9.6;
(2)设生成氯化钾的质量为x
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
149 96
x 9.6g
$\frac{149}{x}=\frac{96}{9.6g}$
x=14.9g
答:反应后剩余固体中氯化钾的质量为14.9g;
(3)充分反应后混合物含KCl、MnO2,MnO2不溶于水,KCl溶于水,从剩余物中回收干燥的二氧化锰,则溶解、过滤、洗涤、干燥.
答案:
(1)生成氧气的质量为9.6g;
(2)反应后剩余固体中氯化钾的质量为14.9g;
(3)过滤.
点评 做本题的关键是要分析出试管内质量的减少量就是生成的氧气质量,再根据氧气质量进行进一步计算.

练习册系列答案
相关题目
9.第31届奥运会于2016年8月5日-8月21日在巴西里约热内卢举行,下列运动设施中用到金属材料的是( )
| A. | 跑步、跳远使用的塑胶跑道 | B. | 排球、羽毛球使用的化纤网 | ||
| C. | 单杠、双杠使用的钢制横梁 | D. | 跳高、拳击使用的海绵护垫 |
10.为相对原子质量的测定作出卓越贡献,主持测定了铟、铱等相对原子质量新值的科学家是( )
| A. |  侯德榜 | B. |  拉瓦锡 | C. |  门捷列夫 | D. |  张青莲 |
7.下列图象中有关量的变化趋势与对应叙述关系正确的是( )
| A. | 分别向盛有等质量铝粉和镁粉的两个烧杯中,不断滴加等浓度的稀硫酸.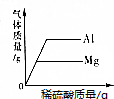 | |
| B. | 在密闭容器中点燃一定量的氢气和氧气的混合气体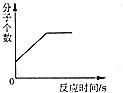 | |
| C. | 向硝酸银、硝酸铜混合溶液中加入一定量的锌粉,充分反应后过滤,得到无色液体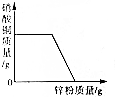 | |
| D. | 向一定量的稀盐酸中不断加入石灰石粉末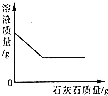 |
14.分析推理是化学学习过程中的常用方法,下列推理正确的是( )
| A. | 化合物含有不同元素的纯净物,所以含有不同种元素的纯净物一定是化合物 | |
| B. | 分子、原子可以构成物质,所以物质一定是由分子、原子构成的 | |
| C. | 可燃物燃烧时温度需要达到着火点,所以可燃物的温度达到着火点一定能燃烧 | |
| D. | 物质和氧气发生的反应是氧化反应,所以发生氧化反应一定有氧气参加 |
4.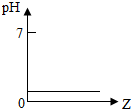 向稀盐酸中加入Z物质,其pH变化情况如图所示,则Z物质是( )
向稀盐酸中加入Z物质,其pH变化情况如图所示,则Z物质是( )
 向稀盐酸中加入Z物质,其pH变化情况如图所示,则Z物质是( )
向稀盐酸中加入Z物质,其pH变化情况如图所示,则Z物质是( )| A. | H2O | B. | AgNO3固体 | C. | 浓盐酸 | D. | KOH固体 |
11.人体中发生的以下变化属于物理变化的是( )
| A. | 汗水的挥发 | B. | 蛋白质的水解 | C. | 葡萄糖的氧化 | D. | 油脂的消化吸收 |
9.如表是根据一些反应事实或现象推理得出的影响化学反应的主要因素,其中不合理的是( )
| 选项 | 化学反应事实(或现象) | 影响因素 |
| A | 过氧化氢在常温下分解速度比较慢,加入二氧化锰后迅速分解 | 催化剂 |
| B | 食物在冰箱中保存不易变质 | 温度 |
| C | 蜡烛在空气中燃烧发出黄色火焰,在纯氧中燃烧火焰明亮 | 反应物的种类 |
| D | 细铁丝在空气中不能燃烧,在纯氧中剧烈燃烧火星四射 | 反应物的浓度 |
| A. | A | B. | B | C. | C | D. | D |