题目内容
14.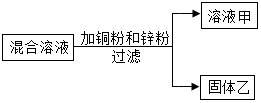 某化学小组用一定量AgNO3和Mg(NO3)2的混合溶液进行了如图所示实验,已知溶液甲呈浅绿色.
某化学小组用一定量AgNO3和Mg(NO3)2的混合溶液进行了如图所示实验,已知溶液甲呈浅绿色.(1)向固体乙中滴加稀盐酸时可能有(填“一定有”、“可能有”或“没有”)气泡产生.
(2)溶液甲中一定含有哪些溶质?Mg(NO3)2、Zn(NO3)2、Fe(NO3)2(写化学式)
(3)写出该实验过程中任意一个反应的化学方程式Zn+2AgNO3=Zn(NO3)2+2Ag,或Fe+2AgNO3=Fe(NO3)2+2Ag.
分析 镁比锌活泼,锌比铁活泼,铁比银活泼,AgNO3和Mg(NO3)2的混合溶液中加入铁和锌时,锌先和硝酸银反应生成硝酸锌和银,锌完全反应后如果硝酸银有剩余,则铁再和硝酸银反应生成硝酸亚铁和银.
解答 解:镁比锌活泼,锌比铁活泼,铁比银活泼,AgNO3和Mg(NO3)2的混合溶液中加入铁和锌时,锌先和硝酸银反应生成硝酸锌和银,锌完全反应后如果硝酸银有剩余,则铁再和硝酸银反应生成硝酸亚铁和银,溶液甲呈浅绿色,说明锌已经完全反应,铁可能是完全反应,也可能是部分反应;
(1)如果铁完全反应,则固体中不含有铁,向固体乙中滴加稀盐酸时不产生气泡,如果铁部分反应,则固体中含有铁,滴加稀盐酸时产生气泡.
故填:可能有.
(2)溶液甲中一定含有的溶质是没有反应的硝酸镁、反应生成的硝酸锌和硝酸亚铁,化学式分别是Mg(NO3)2、Zn(NO3)2、Fe(NO3)2.
故填:Mg(NO3)2、Zn(NO3)2、Fe(NO3)2.
(3)该实验过程中,锌和硝酸银反应生成硝酸锌和银,铁和硝酸银反应生成硝酸亚铁和银,反应的化学方程式分别是:
Zn+2AgNO3=Zn(NO3)2+2Ag、Fe+2AgNO3=Fe(NO3)2+2Ag.
故填:Zn+2AgNO3=Zn(NO3)2+2Ag,或Fe+2AgNO3=Fe(NO3)2+2Ag.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
5. 小红发现实验台上有两瓶标签破损的无色溶液(如图所示),询问老师,确认溶液是初中化学实验用剩的两种化学试剂.于是她对溶液的成分进行了以下探究.
小红发现实验台上有两瓶标签破损的无色溶液(如图所示),询问老师,确认溶液是初中化学实验用剩的两种化学试剂.于是她对溶液的成分进行了以下探究.
【提出问题】这两瓶试剂分别是什么?
【作出猜想】可能是NaOH溶液、Na2CO3溶液、NaHCO3溶液、NaCl溶液、Na2SO4溶液中的任意两种.
【查阅资料】①Na2CO3溶液、NaHCO3溶液呈碱性,NaCl溶液、Na2SO4溶液呈中性;
②碳酸氢钙可溶于水;
③2NaHCO3+Ca(OH)2═CaCO3↓+Na2CO3+2H2O
【设计方案并进行实验】分别取少量瓶中溶液进行以下实验;
【实验反思】小红经过分析认为1号溶液还可能是变质的氢氧化钠溶液,写出氢氧化钠溶液变质的化学方程式2NaOH+CO2═Na2CO3+H2O.
 小红发现实验台上有两瓶标签破损的无色溶液(如图所示),询问老师,确认溶液是初中化学实验用剩的两种化学试剂.于是她对溶液的成分进行了以下探究.
小红发现实验台上有两瓶标签破损的无色溶液(如图所示),询问老师,确认溶液是初中化学实验用剩的两种化学试剂.于是她对溶液的成分进行了以下探究.【提出问题】这两瓶试剂分别是什么?
【作出猜想】可能是NaOH溶液、Na2CO3溶液、NaHCO3溶液、NaCl溶液、Na2SO4溶液中的任意两种.
【查阅资料】①Na2CO3溶液、NaHCO3溶液呈碱性,NaCl溶液、Na2SO4溶液呈中性;
②碳酸氢钙可溶于水;
③2NaHCO3+Ca(OH)2═CaCO3↓+Na2CO3+2H2O
【设计方案并进行实验】分别取少量瓶中溶液进行以下实验;
| 实验步骤 | 实验现象 | 实验结论 |
实验1:分别测定两种溶液的pH 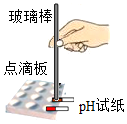 | 两种溶液的pH均大于7 | 两瓶溶液一定不是NaCl溶液、Na2SO4溶液 |
实验2: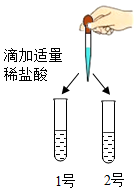 | 均有气泡产生 | 两瓶溶液分别是NaHCO3溶液和Na2CO3溶液.写出Na2CO3溶液与盐酸反应的化学方程式Na2CO3+2HCl═2NaCl+H2O+CO2↑. |
实验3:滴加适量氯化钙溶液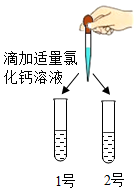 | 1号试管中出现白色沉淀,2号试管中无明显现象 | 1号溶液是Na2CO3溶液 2号溶液是NaHCO3溶液. |
2.在欧洲,花青素(C15H11O6)被称为“口服的皮肤化妆品”,它不但能防止皮肤皱纹的提早生成,更能补充营养和消除体内的有害自由基.下列关于花青素的说法正确的是( )
| A. | 花青素是一种氧化物 | B. | 花青素中氧元素的质量分数最小 | ||
| C. | 一个花青素分子由31个原子构成 | D. | 花青素由碳、氢、氧三种元素组成 |
19.某同学利用下图所示装置探究燃烧的条件(热水温度远高于白磷着火点).下列说法错误的是( )


| A. | 图①烧杯中水的温度应与②中相同 | |
| B. | 图②中白磷燃烧,产生大量白烟 | |
| C. | ①和③对比可以得出燃烧条件之一是“可燃物必须与氧气接触” | |
| D. | ②和③对比可以得出燃烧条件之一是“可燃物的温度必须达到着火点” |
3.逻辑推理是一种重要的化学思维方法,下列推理不合理的是( )
| A. | 有些金属与酸反应产生气体,但与酸反应产生气体的不一定是金属 | |
| B. | 酸的组成中含有氢元素,但含有氢元素的化合物不一定是酸 | |
| C. | 化学变化中分子发生改变,但分子发生改变的变化不一定是化学变化 | |
| D. | 离子是带电的原子或原子团,但带电的粒子不一定是离子 |
4.金属钛(Ti)抗腐蚀性能好,露置于空气中数年,仍光亮如初,以金红石(主要成分是TiO2)为原料生产金属钛的步骤主要有:①在高温下,向金红石与焦炭的混合物中通入氯气(Cl2),得到TiCl4和一种可燃性气体;②在稀有气体环境和加热条件下,用Mg和TiCl4反应得到Ti和MgCl2,下列说法正确的是( )
| A. | ①中的反应TiO2+C+2Cl2$\frac{\underline{\;高温\;}}{\;}$TiCl4+CO2 | |
| B. | ②中的稀有气体的作用是隔绝空气 | |
| C. | ②中发生的反应为置换反应 | |
| D. | 金属钛在常温下易与O2反应 |
 表示氢原子 用
表示氢原子 用 表示氧原子,下列模型能表示变成了水蒸汽的这部分水分子的是( )
表示氧原子,下列模型能表示变成了水蒸汽的这部分水分子的是( )


