题目内容
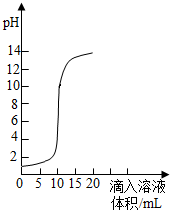
如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线。

(1)氢氧化钠和盐酸恰好完全反应时,溶液的pH 7(填“大于”或“小于”或“等于”)。
(2)根据曲线判断,该反应是将 (填“氢氧化钠溶液”或“盐酸”,下同)滴入 中,理由是 。
(3)当滴入溶液的体积为5mL时,所得溶液中的溶质为 (写化学式),若在此溶液中滴入石蕊试液,溶液显 色。
【答案】
(1)等于(或“=”)
(2)氢氧化钠溶液(或NaOH溶液、NaOH等) 盐酸 (或HCl) 随着滴入溶液的增加,溶液的pH增大
(3)NaCl HCl 红
【解析】
试题分析:(1)氢氧化钠和盐酸恰好完全反应时,溶液呈中性,PH=7 ;
(2)根据曲线,曲线的起点小于7,即起始溶液呈酸性,故是将氢氧化钠溶液滴入稀盐酸中;
(3)由图可知当滴入溶液的体积为5mL时,溶液呈酸性,说明稀盐酸过量,那么所得溶液中的溶质由反应生成的氯化钠和过量的盐酸;酸性溶液能使紫色石蕊溶液变红。
考点:化学反应中溶液PH的变化

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
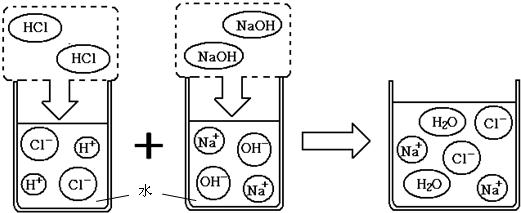
 26、了解物质构成的微观奥秘,能帮助我们更好地认识物质变化的本质.
26、了解物质构成的微观奥秘,能帮助我们更好地认识物质变化的本质.
 分别表示N2、H2、NH3三种分子.为了便于理解,我们将在固体催化剂表面(用
分别表示N2、H2、NH3三种分子.为了便于理解,我们将在固体催化剂表面(用 表示)合成氨的过程简化为下图中的五个步骤,请按照正确的步骤进行排序
表示)合成氨的过程简化为下图中的五个步骤,请按照正确的步骤进行排序






 (2012?桂林)如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.
(2012?桂林)如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.