题目内容
6.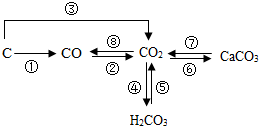 如图是部分含碳物质的转化关系图,根据图示判断下列说法正确的是( )
如图是部分含碳物质的转化关系图,根据图示判断下列说法正确的是( )| A. | ①②③⑧都只能通过化合反应实现 | |
| B. | ⑤⑦均可用于实验室制取CO2 | |
| C. | 将CO2通入紫色石蕊溶液中,溶液变红,可用④来解释原因 | |
| D. | 图中物质均为含碳元素的化合物 |
分析 A、化合反应:两种或两种以上物质反应后生成一种物质的反应,其特点可总结为“多变一”.
B、根据实验室制取CO2的反应原理,进行粉判断.
C、根据二氧化碳的化学性质,进行分析判断.
D、由不同种元素组成的纯净物是化合物.
解答 解:A、①⑧只能通过化合反应实现,②③不一定只能通过化合反应实现,还分别能通过一氧化碳与氧化铜在加热条件下生成铜和二氧化碳、碳与氧化铜在高温条件下生成铜和二氧化碳等来实现,故选项说法错误.
B、实验室常用石灰石与稀盐酸反应制取二氧化碳,同时生成氯化钙、水,不能通过碳酸分解的方法制取,故选项说法错误.
C、将CO2通入紫色石蕊溶液中,溶液变红,原因是二氧化碳与水反应生成碳酸,碳酸使紫色石蕊溶液变红色,可用④来解释原因,故选项说法正确.
D、图中物质中C属于碳的单质,故选项说法错误.
故选:C.
点评 本题难度不大,熟练掌握二氧化碳、一氧化碳、碳的化学性质与实验室制取CO2的反应原理等是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.在一定条件下,甲和乙反应生成丙的微观示意图如下,则下列说法中错误的是( )


| A. | 参加反应的甲、乙两种物质质量比为7:4 | |
| B. | 反应前后分子的个数没有改变 | |
| C. | 一个X分子中含有三个原子 | |
| D. | 该反应属于化合反应 |
8.下列各组物质中的分类正确的是( )
| A. | 氧化物:H2O、NO2、Fe3O4 | B. | 碱:Ca(OH)2、Ba(OH)2、Na2CO3 | ||
| C. | 酸:CH3COOH、CH4、H2SO4 | D. | 盐:NH4NO3、MgCl2、CuO |
18. 实验室有一瓶标签受到腐蚀的无色溶液,如图所示.这瓶无色溶液是放在存放盐溶液的柜子里.化学兴趣小组开展探究:
实验室有一瓶标签受到腐蚀的无色溶液,如图所示.这瓶无色溶液是放在存放盐溶液的柜子里.化学兴趣小组开展探究:
【提出问题】这瓶无色溶液究竟是什么盐的溶液?
【猜想与假设】该无色溶液可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中某一种的溶液.
【初步分析】
(1)库尔班同学根据标签上的组成元素认为一定不是氯化钠溶液.
(2)艾力同学提出,碳酸氢钠、硝酸钠的溶液也不可能,他的依据是碳酸氢钠和硝酸钠的化学式中钠元素右下角的数字为1.
【设计实验】为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如下实验.
【实验结论】
(3)该瓶无色溶液的溶质是Na2CO3(填化学式).生成白色沉淀的化学反应方程式是Na2CO3+BaCl2=BaCO3↓+2NaCl.
【实验反思】
(4)玉素甫同学认为原设计的实验还可简化,同样达到鉴别的目的.丙同学设计的实验如下(将实验操作及实验现象填入相应的空格中):
(5)白燕同学经查阅资料得知:氯化钠、硫酸钠、硝酸钠溶液呈中性,碳酸钠、碳酸氢钠溶液呈碱性,提出测溶液的酸碱性来确定更简便.她采用pH试纸测量溶液的pH值>7(填>、=、<),则结论与以上同学一致.
 实验室有一瓶标签受到腐蚀的无色溶液,如图所示.这瓶无色溶液是放在存放盐溶液的柜子里.化学兴趣小组开展探究:
实验室有一瓶标签受到腐蚀的无色溶液,如图所示.这瓶无色溶液是放在存放盐溶液的柜子里.化学兴趣小组开展探究:【提出问题】这瓶无色溶液究竟是什么盐的溶液?
【猜想与假设】该无色溶液可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中某一种的溶液.
【初步分析】
(1)库尔班同学根据标签上的组成元素认为一定不是氯化钠溶液.
(2)艾力同学提出,碳酸氢钠、硝酸钠的溶液也不可能,他的依据是碳酸氢钠和硝酸钠的化学式中钠元素右下角的数字为1.
【设计实验】为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如下实验.
| 实验操作 | 实验现象 |
| ①取少重该无色溶液于试管中,慢慢滴加BaCl2溶液 ②静置后,向沉淀中滴加稀盐酸 | 产生白色沉淀 产生大量气泡,沉淀全部溶解. |
(3)该瓶无色溶液的溶质是Na2CO3(填化学式).生成白色沉淀的化学反应方程式是Na2CO3+BaCl2=BaCO3↓+2NaCl.
【实验反思】
(4)玉素甫同学认为原设计的实验还可简化,同样达到鉴别的目的.丙同学设计的实验如下(将实验操作及实验现象填入相应的空格中):
| 实验操作 | 实验现象 |
| 取上述无色溶液少许于试管中,滴加少量的稀盐酸 | 溶液中没有气泡产生(或有气泡产生),该瓶无色溶液是硫酸钠溶液(或碳酸钠溶液) |
15. 分类法是化学学习中常用的方法之一,如图是根据组成元素不同对化学肥料的分类概念图,下列叙述错误的是( )
分类法是化学学习中常用的方法之一,如图是根据组成元素不同对化学肥料的分类概念图,下列叙述错误的是( )
 分类法是化学学习中常用的方法之一,如图是根据组成元素不同对化学肥料的分类概念图,下列叙述错误的是( )
分类法是化学学习中常用的方法之一,如图是根据组成元素不同对化学肥料的分类概念图,下列叙述错误的是( )| A. | CO(NH2)2、氨水、硝酸铵属于氮肥 | B. | 硫酸钾、氯化钾、硝酸钾属于钾肥 | ||
| C. | 图中①表示的是磷肥 | D. | 图中②表示复合肥 |
16.下列说法错误的是( )
| A. | 自来水厂净水过程包括沉淀、过滤、吸附、消毒 | |
| B. | 合金一般比组成它们的纯金属的硬度大、熔点低 | |
| C. | 硒有防癌、抗癌的作用,人体必需大量补硒 | |
| D. | 质量守恒定律适用于所有的化学反应 |