题目内容
下列除去杂质(少量)的方法中,正确的是( )
选项 物质 杂质 除杂方法
A H2 HCl 通过饱和的 Na2CO3溶液
B KNO3晶体 NaCl 高温下制成饱和溶液,降温结晶,过滤,洗涤烘干
C NaCl晶体 Na2CO3 加稍过量稀盐酸,蒸发结晶
D KCl溶液 K2SO4 加稍过量Ba(NO3)2溶液,过滤
A. A B. B C. C D. D
解:A、HCl能与饱和的 Na2CO3溶液反应生成氯化钠、水和二氧化碳,能除去杂质但引入了新的杂质二氧化碳,不符合除杂原则,故选项所采取的方法错误.
B、KNO3和NaCl的溶解度受温度的影响不同,硝酸钾溶解度受温度影响较大,而氯化钠受温度影响较小,所以可采取加热水溶解配成饱和溶液、降温结晶使KNO3先结晶出来、再过滤的方法;故选项所采取的方法错误.
C、Na2CO3能与稍过量稀盐酸反应生成氯化钠、水和二氧化碳,再蒸发结晶(除去稀盐酸和水分),能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、K2SO4能与稍过量Ba(NO3)2溶液反应生成硫酸钡沉淀和硝酸钾,能除去杂质但引入了新的杂质硝酸钾、硝酸钡(过量的),不符合除杂原则,故选项所采取的方法错误.
故选:C.

 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
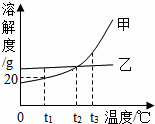
ABC考王全优卷系列答案甲、乙两种不含结晶水的固体物质的溶解性曲线如图,下列说法中正确的是( )
|
| A. | 甲的溶解度比乙大 |
|
| B. | t1℃时,甲的饱和溶液中溶质与溶液的质量比为1:5 |
|
| C. | t2℃时,甲、乙两种饱和溶液中溶质的质量分数相等 |
|
| D. | 将等质量甲、乙的两种溶液分别由t3℃降温至t2℃,析出甲的质量一定比析出乙的质量大 |
溶解度曲线是物质溶解性的直观体现,如图是a,b,c三种物质的溶解度曲线,下列说法正确的是( )
|
| A. | a物质的溶解度大于b物质 |
|
| B. | c物质的溶解度随温度的升高而增大 |
|
| C. | 使b物质结晶析出主要采用降温的方法 |
|
| D. | t2℃时,a,b两种物质饱和溶液的溶质质量分数相等 |
能保持氧化汞的化学性质的最小粒子是( )
|
| A. | 汞原子和氧原子 | B. | 氧化汞分子 | C. | 汞原子 | D. | 氧原子 |
保持氧气的化学性质的最小粒子是( )
|
| A. | 氧原子 | B. | 氧分子 | C. | 氧元素 | D. | 氧离子 |

