题目内容
12.除去下列各物质中含有少量杂质的方法,不合理的是( )| 选项 | 物质 | 所含杂质 | 除去杂质的办法 |
| A | N2 | O2 | 通过足量的灼热铜网 |
| B | CO | CO2 | 通过足量的氢氧化钠溶液 |
| C | H2 | 水蒸气 | 通过盛有硫酸铜粉末的干燥管 |
| D | CO2 | CO | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、氧气通过灼热的铜网时可与铜发生反应生成氧化铜,而氮气不与铜反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
B、CO2能与氢氧化钠溶液反应生成碳酸钠和水,CO不与氢氧化钠溶液反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
C、硫酸铜粉末能与水蒸气反应生成五水合硫酸铜,氢气不与硫酸铜粉末反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、除去二氧化碳中的一氧化碳不能够点燃,这是因为当二氧化碳(不能燃烧、不能支持燃烧)大量存在时,少量的一氧化碳是不会燃烧的;故选项所采取的方法错误.
故选:D.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案
相关题目
20.足量的盐酸分别与等质量的铁、镁、铝三种金属完全反应,所得氢气质量最多的是( )
| A. | 铁 | B. | 镁 | C. | 铝 | D. | 无法确定 |
7.小华想测定Cu-Zn合金和Cu-Ag合金中铜的质量分数,实验室只提供了一瓶稀盐酸和相关的仪器.
(1)根据现有的条件,你认为只能测出Cu-Zn合金中铜的质量分数.
(2)为了测定该合金的组成,小华称取10g该合金粉末,在粉末中连续三次加入稀盐酸反应.每加一次盐酸,小华记录所得气体的质量,实验数据如下:
①从上表数据分析,小华用10g合金粉末总共收集到氢气0.2g.
②该合金中铜的质量分数为35%.(H-1 Cu-64 Zn-65 Ag-108 Cl-35.5)
③求所用盐酸中溶质的质量分数.
④求完全反应时所得溶液的溶质的质量分数.
(1)根据现有的条件,你认为只能测出Cu-Zn合金中铜的质量分数.
(2)为了测定该合金的组成,小华称取10g该合金粉末,在粉末中连续三次加入稀盐酸反应.每加一次盐酸,小华记录所得气体的质量,实验数据如下:
| 第一次 | 第二次 | 第三次 | |
| 连续加入盐酸的体积(mL) | 10 | 10 | 10 |
| 生成氢气的质量(g) | 0.08 | 0.08 | 0.04 |
②该合金中铜的质量分数为35%.(H-1 Cu-64 Zn-65 Ag-108 Cl-35.5)
③求所用盐酸中溶质的质量分数.
④求完全反应时所得溶液的溶质的质量分数.
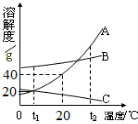 如图为A、B、C三种物质的溶解度曲线,据图回答:
如图为A、B、C三种物质的溶解度曲线,据图回答: 化学与生活息息相关.
化学与生活息息相关.