题目内容
化学兴趣小组的李浩宇同学对“一贴热”的发热原理产生了浓厚的兴趣,他先上网查阅有关资料,然后和兴趣小组的同学一起带了几包“一贴热”(如图1),来到实验室对其进行实验研究.

【查阅资料】
(1)一贴热的使用方法:将外包装袋剪开,取出药袋,晃动几次,使药物充分接触到空气,手摸有热感时,置于固定袋内,覆盖于痛患处.
(2)四氧化三铁也具有铁磁性,能被磁铁吸引.
(3)可以作为过氧化氢分解反应的催化剂有很多,如:铁粉、氧化铜粉末、四氧化三铁等.
【提出问题】一贴热的成分是什么?
李浩宇同学将一贴热包装剪开,将填充物倒入烧杯中,观察,为黑色粉末.
【猜想与假设】李浩宇说:该黑色粉末可能含有碳粉、铁粉.
你猜想该黑色粉末还可能是 (与李浩宇的猜想不同)
【设计并进行试验】
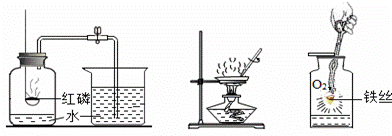
如图2(1)先用磁铁与烧杯中的黑色粉末充分接触,如果粉末部分被吸附,你认为该黑色粉末可能是① ;② .
(2)王梅取适量黑色粉末于燃烧匙中,在酒精灯上点燃后伸入盛有氧气的集气瓶中,观察到剧烈燃烧、火星四射、放出大量热、 的现象,从而证明了铁粉的存在.写出铁与氧气反应的文字表达式 .在反应后的集气瓶中加入澄清的石灰水振荡,观察到石灰水变浑浊,说明粉末中一定含有 .
【实验结论】
该黑色粉末中一定含有 ,可能含有 .
张阳和厂家联系得知,一贴热的发热材料主要由铁粉、活性炭、蛭石、水、盐等材料构成.
【拓展探究】
(1)二氧化锰和铁粉,谁能更好的加快过氧化氢分解反应的速率?
冯伟经过实验发现一贴热也可以加快过氧化氢分解的速率,经检验是铁粉起的作用,他想知道铁粉和二氧化锰相比,究竟谁的催化效果更好,于是设计以下一组实验:
| 实验编号 | 反应物的浓度体积 | 温度 | 催化剂 | 收集125ml 氧气所用的时间 |
| 1 | 10mL 6% H2O2 | 25℃(室温) | 1g 二氧化锰粉末 | 35s |
| 2 | 10mL 6% H2O2 | 25℃(室温) | 1g 铁粉 | 152s |
根据控制变量法,上表中变量是: ,常量是 、 、 (至少写出三个).由该实验可以得出:在相同条件下,二氧化锰的催化效果比铁粉 .(填“好”或“差”)
(2)用一贴热药粉测定空气中氧气的含量.王岚查阅资料得知,一贴热的作用原理是铁跟氧气和水发生反应生成氢氧化铁(固体),并放热.小组同学设计了如图2所示的实验装置,进行实验.请你仔细观察并在下表中填写主要的实验现象.
| 实验操作 | 主要实验现象 | 实验结论及解释 |
| 加入足量药品一贴热,迅速将胶塞盖严,并充分振荡 | 进入集气瓶内水的体积即为空气中氧气的体积,并可计算空气中氧气的含量 |
(你能回答下列问题,可获得3分的加分,但总分不超过100分)
【实验反思】王岚同学认为实验需要改进,才能得到较为准确的结果.试写出改进的实验操作: .
| 实验探究物质的组成成分以及含量;催化剂的特点与催化作用;常见金属的特性及其应用;金属的化学性质;书写化学方程式、文字表达式、电离方程式.. | ||||||||||||||||||||||||||||
| 专题: | 科学探究. | |||||||||||||||||||||||||||
| 分析: | 【猜想与假设】考虑初中化学中黑色粉末有哪些物质,提纯合理的猜想; 【设计并进行试验】如图2(1)考虑磁铁的性质,推测该黑色粉末可能的组成. (2)考虑铁粉在氧气中燃烧的现象,从而证明了铁粉的存在.考虑二氧化碳的鉴别方法. 【实验结论】根据【设计并进行试验】中的实验现象,推测该黑色粉末成分. 【拓展探究】 (1)考虑实验中的变量和常量;根据表格中的数据,推测二氧化锰和铁粉的催化效果; (2)根据实验操作和实验结论及解释,根据题目中的信息“一贴热的作用原理是铁跟氧气和水发生反应生成氢氧化铁(固体),并放热”,推测主要的实验现象. 【实验反思】推测改进的实验操作:关闭弹簧夹a后加入足量药品,迅速将胶塞盖紧,充分振荡,待冷却后打开弹簧夹a. | |||||||||||||||||||||||||||
| 解答: | 解: 【猜想与假设】考虑初中化学中黑色粉末有哪些物质,该黑色粉末可能含有四氧化三铁;二氧化锰;碳粉、铁粉、四氧化三铁的混合物、氧化铜.则猜想该黑色粉末还可能是四氧化三铁; 【设计并进行试验】考虑磁铁吸铁,如图2(1)先用磁铁与烧杯中的黑色粉末充分接触,如果粉末部分被吸附,则该黑色粉末可能是①铁粉与碳粉的混合物;②四氧化三铁与炭粉的混合物. (2)取适量黑色粉末于燃烧匙中,在酒精灯上点燃后伸入盛有氧气的集气瓶中,观察到剧烈燃烧、火星四射、放出大量热、生成黑色固体的现象,从而证明了铁粉的存在.则铁与氧气反应的文字表达式铁+氧气 【实验结论】 根据以上分析,可知该黑色粉末中一定含有铁粉和碳粉,可能含有四氧化三铁粉末. 【拓展探究】 (1)根据实验表格中的数据可知:
根据控制变量法,上表中变量是:催化剂的种类,常量是反应物的浓度、体积、温度.由该实验可以得出:在相同条件下,二氧化锰的催化效果比铁粉好. (2)根据资料“一贴热的作用原理是铁跟氧气和水发生反应生成氢氧化铁(固体),并放热”.则推测出主要的实验现象.
【实验反思】王岚同学认为实验需要改进,才能得到较为准确的结果.试写出改进的实验操作:关闭弹簧夹a后加入足量药品,迅速将胶塞盖紧,充分振荡,待冷却后打开弹簧夹a. 故答案为: 【猜想与假设】四氧化三铁;二氧化锰;碳粉、铁粉、四氧化三铁的混合物、氧化铜(只要答黑色粉末状一种物质均可) 【设计并进行实验】①铁粉与碳粉的混合物;②四氧化三铁与炭粉的混合物;生成黑色固体;铁+氧气 【实验结论】铁粉和碳粉; 四氧化三铁粉末; 【拓展研究】(1)催化剂的种类(如果只写催化剂不得分);(2)反应物的浓度、体积、温度;
(提示:放热,导气管口有气泡冒出只要答出一点可得;一段时间后,量筒中的水沿着导管逐渐被吸入到集气瓶中,只要意思对就可得) 实验改进:关闭弹簧夹a后加入足量药品,迅速将胶塞盖紧,充分振荡,待冷却后打开弹簧夹a | |||||||||||||||||||||||||||
| 点评: | 该题为综合实验题,考查的知识点较多,氧气的性质,装置气密性的检验等,关键是熟记相关知识点.语言表述要简练准确.掌握铁的化学性质,空气中氧气含量的测定. |

 备战中考寒假系列答案
备战中考寒假系列答案人们在阳光照射的树林里,会感到空气特别清新,其原因是树林里含有少量的氧气被转化成具有消毒杀菌作用的臭氧.下列关于氧气和臭氧的说法正确的是( )
|
| A. | 它们都含氧分子 |
|
| B. | 它们的物理性质和化学性质都相同 |
|
| C. | 由氧气变成臭氧发生化学变化 |
|
| D. | 它们属于同一种物质 |
归纳推理是学习化学的重要方法之一.下列有关事实和推理得到的结论合理的是( )
| 事实 | 推论 | |
| A | 物质都是由元素组成的,同种元素可以组成纯净物 | 则不同元素也可以组成纯净物 |
| B | 铁粉可以在氧气中燃烧 | 铁粉在空气中也能燃烧 |
| C | 在过氧化氢中加入二氧化锰后产生了大量气泡 | 二氧化锰使过氧化氢分解的生成物大大增加了 |
| D | 氧气可以使带火星的木条复燃 | 氧气可以作为燃料 |
|
| A. | A | B. | B | C. | C | D. | D |
下列有关空气各成分的说法正确的是( )
|
| A. | 空气质量报告中所列的空气质量级别越大,空气质量越好 |
|
| B. | 氧气的化学性质比较活泼,属于可燃物 |
|
| C. | 二氧化碳在空气中含量增多会引起温室效应,属于空气污染物 |
|
| D. | 氮气的化学性质不活泼,可用于食品防腐 |
 四氧化三铁.在反应后的集气瓶中加入澄清的石灰水振荡,因为二氧化碳使澄清石灰水变浑浊,故观察到石灰水变浑浊,说明粉末中一定含有碳粉.
四氧化三铁.在反应后的集气瓶中加入澄清的石灰水振荡,因为二氧化碳使澄清石灰水变浑浊,故观察到石灰水变浑浊,说明粉末中一定含有碳粉. 四氧化三铁;碳粉;
四氧化三铁;碳粉;
 可能是(只答一条): _______ 。
可能是(只答一条): _______ 。