题目内容
18. 某化学兴趣小组在做铁与硫酸铜溶液反应实验时,发现生成紫红色固体的同时还伴有少量气泡产生.为了进一步探究,他们又做了如下实验:
某化学兴趣小组在做铁与硫酸铜溶液反应实验时,发现生成紫红色固体的同时还伴有少量气泡产生.为了进一步探究,他们又做了如下实验:①取8.5g纯铁粉放入一定量的硫酸铜溶液中,反应完成后,滤出固体,洗涤、干燥后称量,固体质量为9.2g.
②将9.2g固体与一定质量分数的稀盐酸充分反应后,他们根据实验数据绘制反应产生氢气的质量(g)与反应时间(min)的关系图(如图).
请回答下列问题:
(1)铁与稀盐酸反应的化学方程式为:Fe+2HCl=FeCl2+H2↑.
(2)与硫酸铜反应的铁的质量为5.6g.
(3)整个实验过程中,参与反应的铁的质量之和小于8.5g.由此,你得出的结论是:有少量铁与硫酸铜溶液中的酸性物质反应生成了气体.
分析 (1)铁与盐酸反应生成氯化亚铁和氢气;
(2)利用铁与盐酸反应的化学方程式,根据氢气的质量求出铁的质量.9.2g固体能与盐酸发生反应,说明9.2g固体不全是铜,还有铁,用9.2g-固体中混有的铁的质量=铜的质量.利用铁与硫酸铜反应的化学方程式,根据铜的质量求出铁的质量.
(3)在做铁与硫酸铜溶液反应的实验时,发现生成铜的同时有气泡产生.说明硫酸铜溶液中混有酸,部分铁与硫酸铜溶液中的酸发生反应,所以会造成与硫酸铜反应的铁的质量及与盐酸反应的铁的质量之和小于8.5g.
解答 解:(1)铁与盐酸反应生成氯化亚铁和氢气,化学方程式为:Fe+2HCl=FeCl2+H2↑;
(2)设与盐酸反应的铁的质量为x
Fe+2HCl=FeCl2+H2↑
56 2
x 0.1g
$\frac{56}{x}=\frac{2}{0.1g}$
x=2.8g
9.2g固体中铜的质量为:9.2g-2.8g=6.4g
设与硫酸铜反应的铁的质量为y
Fe+CuSO4=FeSO4+Cu
56 64
y 6.4g
$\frac{56}{y}=\frac{64}{6.4g}$
y=5.6g
答:和硫酸铜反应的铁的质量为5.6g.
(3)2.8g+5.6g=8.4g<8.5g
故答案为:有少量铁与硫酸铜溶液中的酸性物质反应生成了气体.
点评 做硫酸铜与铁反应的实验时,生成的铜覆盖在铁的表面,会造成铁不能完全反应,所以将生成的铜放入盐酸中会有气体生成,那其实是未反应的铁在与盐酸发生反应.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
8.用CO2和NH3合成尿素,是固定和利用CO2的成功范例,尿素的化学式为CO(NH2)2.其反应的化学方程式为:CO2+2NH3═CO(NH2)2+H2O.下列说法正确的是( )
| A. | 尿素中有2个氮原子 | |
| B. | 尿素中碳、氧、氮、氢元素的质量比为3:4:7:1 | |
| C. | 参加反应的CO2与NH3的质量比是44:17 | |
| D. | 该反应是充分利用CO2的一种有效途径 |
6.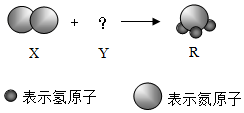 如图所示,一个X分子和三个Y分子反应生成两个R分子,则从图示获得的信息中,错误的是( )
如图所示,一个X分子和三个Y分子反应生成两个R分子,则从图示获得的信息中,错误的是( )
 如图所示,一个X分子和三个Y分子反应生成两个R分子,则从图示获得的信息中,错误的是( )
如图所示,一个X分子和三个Y分子反应生成两个R分子,则从图示获得的信息中,错误的是( )| A. | 该反应属于化合反应 | |
| B. | 反应前后原子的种类发生了改变 | |
| C. | 反应的化学方程式为N2+3H2═2NH3 | |
| D. | 反应前后,氮、氢两种原子的化合价都发生了改变 |
3.临沂市某日的空气质量日报如表:
(1)据图所示,该日临沂市的主要污染物是可吸入颗粒物.
(2)下列情况对表中三个空气质量指标不会产生影响的是A(填字母序号).
A.利用风力发电 B.露天焚烧垃圾 C.用煤作燃料.
| 项目 | 空气污染指数 | 空气质量级别 | 空气质量 |
| 可吸入颗粒物 | 65 | Ⅱ | 良 |
| 二氧化硫 | 6 | ||
| 二氧化氮 | 20 |
(2)下列情况对表中三个空气质量指标不会产生影响的是A(填字母序号).
A.利用风力发电 B.露天焚烧垃圾 C.用煤作燃料.
8.下列实验操作中,可能会造成安全事故的是( )
| A. | 用嘴吹灭酒精灯 | B. | 先预热,再给试管内的物质加热 | ||
| C. | 扇闻气体的气味 | D. | 取用液体时细口瓶标签对着手心 |