题目内容
15.如表是NaOH的溶解度数据,请回答下列问题:| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 31 | 90 | 111 | 130 | 313 | 336 |
(2)20℃时,95gNaOH的饱和溶液加入130g水可得到20%的溶液.
分析 (1)根据氢氧化钠溶于水放热以及氢氧化钠的溶解度来分析;
(2)根据溶液加水稀释过程中溶质的质量不变来分析解答.
解答 解:(1)氢氧化钠固体溶于水后会放出热量,所以把氢氧化钠固体放入水中时,溶液的温度会升高;由表格信息可知,在20℃时,氢氧化钠的溶解度为90g,也就是该温度下,100g水中溶解90g氢氧化钠达到饱和状态,则该温度下的20g水中恰好溶解18g氢氧化钠达到饱和,所以充分溶解后再降温至20℃,NaOH固体没有析出;故填:NaOH溶于水放出热量;没有;
(2)解:20℃时,95gNaOH的饱和溶液加入水形成20%的溶液时,溶质的质量不变.
设需要加入水的质量为x,则
95g×$\frac{90g}{90g+100g}×100%$=(95g+x)×20%
x=130g
故填:130.
点评 本题考查溶解度及其应用、溶解时的吸热和放热现象等,根据题目的信息可计算出所需水的质量,本考点主要出现在选择题和填空题中.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案
相关题目
20.下列关于空气的说法中,不正确的是( )
| A. | 少量有害气体进入空气中,依靠大自然的自净能力,空气仍能保持洁净 | |
| B. | 空气中的CO2含量过多是导致温室效应的主要原因 | |
| C. | 按质量计算,空气中含氮气78%,氧气21%,其他气体和杂质约占1% | |
| D. | 空气中稀有气体一般不跟其他物质反应,曾被称为“惰性气体” |
7.在元旦联欢晚会上,小明同学在化学老师的指导下,表演了“吹气生火”的魔术.他用棉花将淡黄色的过氧化钠(Na2O2)固体包在其中,将一根长玻璃管插入棉花团中吹气,棉花团剧烈燃烧起来.为了揭开魔术的秘密,同学们进行了如下探究.
【提出问题】过氧化钠与人呼出的哪种气体发生反应?
【查阅资料】
①人呼出的气体中主要成分是N2、O2、CO2和水蒸气等.
②氢氧化钠溶液能与CO2反应但与O2不反应.
【作出猜想】
①过氧化钠与人呼出的N2反应并生成O2.
②过氧化钠与人呼出的水蒸气反应并生成O2.
③过氧化钠与人呼出的CO2反应并生成O2.
【进行实验】
【解释与结论】
(1)实验1中,观察到燃着的木条熄灭的现象,可判断猜想①不成立.
(2)由上述3个实验可判断,猜想②、③成立.已知实验2的B装置中反应的另一种产物由三种元素组成,写出该反应的化学方程式2Na2O2+2H2O═4NaOH+O2↑.
(3)实验3的B装置是为了吸收多余的二氧化碳,则该装置中所装的药品为氢氧化钠溶液.
【反思与评价】
根据棉花团(可燃物)剧烈燃烧的现象分析,反应中除了生成氧气外,还说明过氧化钠发生的反应是放热(填“吸热”或“放热”)反应.
【提出问题】过氧化钠与人呼出的哪种气体发生反应?
【查阅资料】
①人呼出的气体中主要成分是N2、O2、CO2和水蒸气等.
②氢氧化钠溶液能与CO2反应但与O2不反应.
【作出猜想】
①过氧化钠与人呼出的N2反应并生成O2.
②过氧化钠与人呼出的水蒸气反应并生成O2.
③过氧化钠与人呼出的CO2反应并生成O2.
【进行实验】
| 序号 | 实验装置 | 实验现象 |
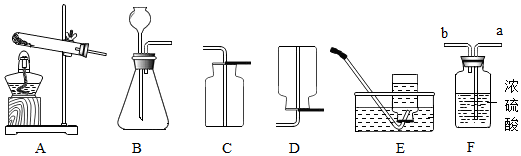
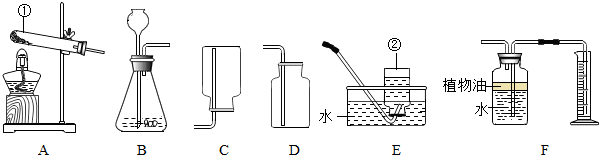
| 实验1 | 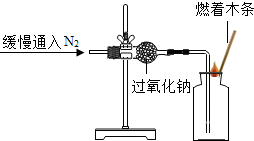 | / |
| 实验2 | 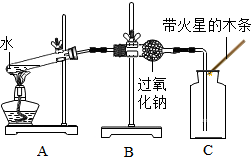 | 带火星的木条复燃 |
| 实验3 | 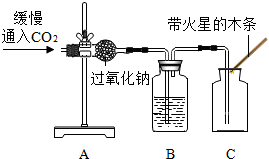 | 带火星的木条复燃 |
(1)实验1中,观察到燃着的木条熄灭的现象,可判断猜想①不成立.
(2)由上述3个实验可判断,猜想②、③成立.已知实验2的B装置中反应的另一种产物由三种元素组成,写出该反应的化学方程式2Na2O2+2H2O═4NaOH+O2↑.
(3)实验3的B装置是为了吸收多余的二氧化碳,则该装置中所装的药品为氢氧化钠溶液.
【反思与评价】
根据棉花团(可燃物)剧烈燃烧的现象分析,反应中除了生成氧气外,还说明过氧化钠发生的反应是放热(填“吸热”或“放热”)反应.
5.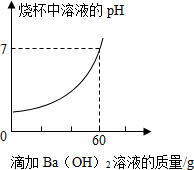 某品牌洁厕灵的成分是硫酸与盐酸的混合溶液,某课外活动小组想测定该品牌洁厕灵溶液中HCl的质量.取20g该品牌的洁厕灵溶液于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,反应过程中烧杯中产生沉淀质量和烧杯中溶液pH变化的部分数据如表所示:(已知BaCl2溶液的pH=7)
某品牌洁厕灵的成分是硫酸与盐酸的混合溶液,某课外活动小组想测定该品牌洁厕灵溶液中HCl的质量.取20g该品牌的洁厕灵溶液于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,反应过程中烧杯中产生沉淀质量和烧杯中溶液pH变化的部分数据如表所示:(已知BaCl2溶液的pH=7)
求:
(1)完全反应后生成沉淀的质量为4.66g;
(2)计算该洁厕灵溶液中HCl的质量分数为多少?(计算结果保留至0.1%)
 某品牌洁厕灵的成分是硫酸与盐酸的混合溶液,某课外活动小组想测定该品牌洁厕灵溶液中HCl的质量.取20g该品牌的洁厕灵溶液于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,反应过程中烧杯中产生沉淀质量和烧杯中溶液pH变化的部分数据如表所示:(已知BaCl2溶液的pH=7)
某品牌洁厕灵的成分是硫酸与盐酸的混合溶液,某课外活动小组想测定该品牌洁厕灵溶液中HCl的质量.取20g该品牌的洁厕灵溶液于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,反应过程中烧杯中产生沉淀质量和烧杯中溶液pH变化的部分数据如表所示:(已知BaCl2溶液的pH=7)| 滴加氢氧化钡溶液的质量/g | 5 | 10 | 25 |
| 烧杯中产生沉淀的质量/g | 1.165 | 2.33 | 4.66 |
(1)完全反应后生成沉淀的质量为4.66g;
(2)计算该洁厕灵溶液中HCl的质量分数为多少?(计算结果保留至0.1%)