题目内容
 如图为哈药集团制药厂生产的“新盖中盖牌”高钙片标签上的部分文字,请仔细阅读后回答下列问题.
如图为哈药集团制药厂生产的“新盖中盖牌”高钙片标签上的部分文字,请仔细阅读后回答下列问题.(1)“新盖中盖牌”高钙片中的“钙”应理解为(填序号)
①元素 ②原子 ③分子 ④氧化物
(2)维生素D种类较多,其中维生素D2的化学式为C28H44O,①维生素D2的相对分子质量是
(3)计算高钙片中碳酸钙的质量分数是多少?
友情提示:(物质的质量分数=该物质的质量/总物质的质量×100%)
考点:标签上标示的物质成分及其含量,元素的概念,相对分子质量的概念及其计算,元素质量比的计算,元素的质量分数计算
专题:标签图示型
分析:(1)食品、药品、营养品、矿泉水等物质中的“钙”等不是以单质、氧化物、分子、原子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述.
(2)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答;根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)由题意,每片含钙元素500mg=0.5g,根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,结合题意进行分析解答
(2)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答;根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)由题意,每片含钙元素500mg=0.5g,根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,结合题意进行分析解答
解答:解:
(1)“新盖中盖牌”高钙片中的“钙”不是以单质、氧化物、分子、原子等形式存在,这里所指的“钙”是强调存在的元素,与具体形态无关.
(2)C28H44O的相对分子质量=12×28+1×44+16=396;
C28H44O中C、H、O三种元素的质量比为:(12×28):(1×44):(16)=84:11:4.
(3)CaCO3的相对分子质量=40+12+16×3=100;
CaCO3中钙元素的质量分数=
×100%=40%;
每片高钙片中含CaCO3的质量=0.5g÷40%=1.25g;
高钙片中碳酸钙的质量分数=
×100%=50%.
答案:
(1)①
(2)396;84:11:4
(3)50%
(1)“新盖中盖牌”高钙片中的“钙”不是以单质、氧化物、分子、原子等形式存在,这里所指的“钙”是强调存在的元素,与具体形态无关.
(2)C28H44O的相对分子质量=12×28+1×44+16=396;
C28H44O中C、H、O三种元素的质量比为:(12×28):(1×44):(16)=84:11:4.
(3)CaCO3的相对分子质量=40+12+16×3=100;
CaCO3中钙元素的质量分数=
| 40 |
| 100 |
每片高钙片中含CaCO3的质量=0.5g÷40%=1.25g;
高钙片中碳酸钙的质量分数=
| 1.25g |
| 2.5g |
答案:
(1)①
(2)396;84:11:4
(3)50%
点评:本题难度不大,以高钙片标签上的部分文字为载体考查了同学们新信息获取、处理及灵活运用化学知识进行分析问题、解决实际问题的能力.

练习册系列答案
相关题目
自然界的水经过沉降、过滤、灭菌等步骤净化处理后,通过管道输送到千家万户成为自来水.关于自来水,下列说法正确的( )
| A、仍含有大量不溶性的杂质 |
| B、是纯净的水,是一种纯净物 |
| C、不含有任何可溶性杂质 |
| D、是仍然可能含有病菌的水,所以要煮沸杀菌后再饮用 |
在三个集气瓶中分别盛有空气、氮气、氧气,鉴别他们的最好方法是( )
| A、用燃着的木条 |
| B、用带火星的木条 |
| C、倒入澄清的石灰水 |
| D、分别称取各自的重量 |
地壳中含量最多的金属元素是( )
| A、铝 | B、铁 | C、硅 | D、氧 |
某矿泉水标签上印有主要成分有:K(1.0~27.0)mg/L;Cl(1.0~24.0)mg/L.这里的K、Cl是指( )
| A、元素 | B、单质 |
| C、金属离子 | D、分子 |
下列物质由原子构成的是( )
| A、氩气 |
| B、氯化钠 |
| C、蒸馏水 |
| D、C60 |
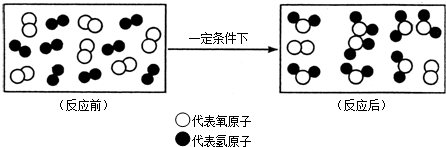
如图所示是某反应前后的微观示意图,“ ”和“
”和“ ”表示两种不同的原子.则该反应( )
”表示两种不同的原子.则该反应( )
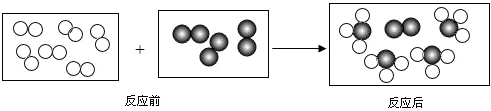
 ”和“
”和“ ”表示两种不同的原子.则该反应( )
”表示两种不同的原子.则该反应( )
| A、是化合反应 |
| B、有单质生成 |
| C、反应前后分子种类不变 |
| D、参加反应的两种分子个数比为4:1 |